A Covid-19 e o microbioma intestinal
Microbiota e Covid-19
Pelo Prof. Tao Zuo
Instituto de Investigação em Gastroenterologia SYSU, Instituto de Investigação em Gastroenterologia de Guangdong, Sexto Hospital Afiliado da Universidade de Sun Yat-Sen, Universidade de Sun Yat-sen (SYSU), Guangzhou, China
Área para o público geral
Encontre aqui o seu espaço dedicado
en_sources_title
en_sources_text_start en_sources_text_end
Capítulos
Sobre este artigo
Autor
A microbiota intestinal, incluindo as frações bacterianas, fúngicas e virais, está a co povoar os intestinos humanos e a regular a imunidade do hospedeiro contra as invasões patogénicas. As composições amplamente heterogéneas da microbiota intestinal (MI) entre indivíduos podem influenciar as respostas imunitárias do hospedeiro à infeção por SARS-CoV-2, levando a vários sintomas e resultados da doença da Covid-19. Por outro lado, embora a infeção por SARS-CoV-2 cause principalmente sintomas respiratórios, desregula profundamente a imunidade sistémica do hospedeiro e tem impacto nos sistemas gastrointestinais onde a microbiota intestinal pode ser afetada tanto a curto como a longo prazo. Aqui, revemos a evidência atual sobre o impacto da Covid-19 na GM humana, bem como as associações entre a composição da MI e a gravidade da Covid-19.
Covid-19 é uma doença respiratória causada por um novo coronavírus (SARSCoV 2) e ainda hoje afeta dezenas de milhões de pessoas em todo o mundo. Embora a maioria dos doentes com Covid-19 apresente sintomas respiratórios, 20% deles apresentam sintomas gastrointestinais (GI), incluindo diarreia [1], o que sugere que o trato digestivo é um local extrapulmonar de expressão da doença e infeção por SARS-CoV-2. Além disso, a Covid-19 apresenta um largo espectro de gravidade da doença, variando desde assintomática, ligeira, grave, e até crítica, resultando em insuficiência respiratória ou mesmo em morte [2].
O trato GI é o maior órgão imunitário do ser humano, desempenhando papéis críticos na defesa do hospedeiro contra infeções patogénicas. Triliões de microrganismos vivem e colonizam o intestino humano - bactérias, fungos, vírus, e outras formas de vida que são coletivamente conhecidas como a microbiota -, regulando a imunidade do hospedeiro. Por conseguinte, é importante compreender se a microbiota intestinal modula a suscetibilidade e gravidade da infeção por SARS-CoV-2, bem como o impacto da infeção por SARS-CoV-2 na Mdo hospedeiro e o seu efeito a longo prazo a jusante na saúde humana.
A microbiota bacteriana e a Covid-19
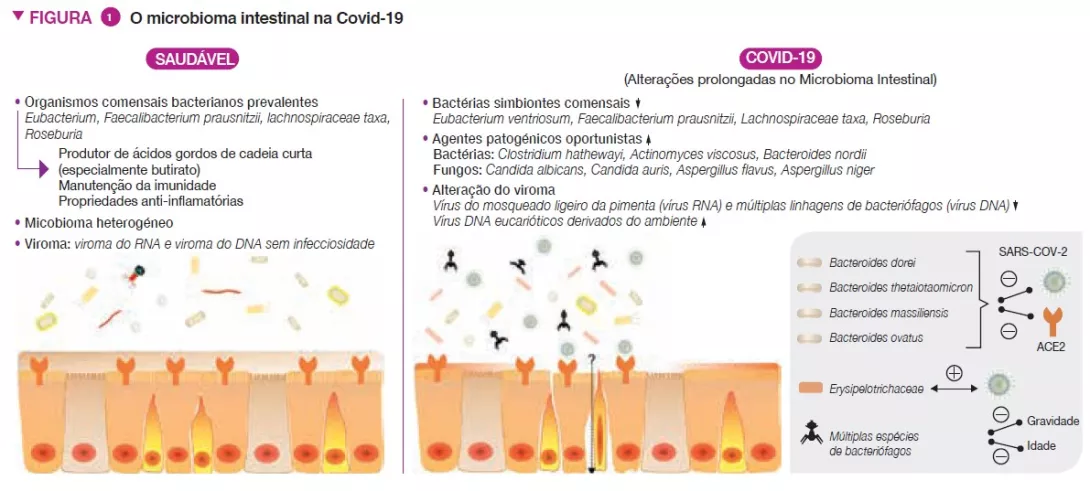
Os doentes que contraíram Covid-19 tiveram alterações significativas no microbioma bacteriano intestinal em comparação com indivíduos saudáveis, caracterizadas pelo esgotamento de organismos comensais benéficos e enriquecimento de agentes patogénicos oportunistas no intestino (Figura 1) [3]. O esgotamento dos simbiontes intestinais persistiu mesmo após a resolução da Covid-19. A abundância de linha de base (na hospitalização) das bactérias Coprobacillus, Clostridium ramosum e Clostridium hathewayi mostrou uma correlação positiva com a gravidade da Covid-19, ao passo que se verificou uma correlação inversa entre a abundância de Faecalibacterium prausnitzii (conhecida como bactéria anti-inflamatória) e a gravidade da doença.
ASARS-CoV-2 utiliza o recetor da enzima conversora da angiotensina 2 (ACE2) para entrar no hospedeiro e este recetor apresenta uma expressão elevada tanto no trato respiratório como gastrointestinal [4]. A ACE2 é importante no controlo da inflamação intestinal e da ecologia microbiana intestinal [5]. Quatro espécies de Bacteroides, B. dorei, B. thetaiotaomicron, B. massiliensis e B. ovatus, foram descritas como estando inversamente associadas à expressão da ACE2 em intestino murino [6]. Curiosamente, a sua abundância no microbioma fecal também mostrou uma correlação inversa com a carga viral fecal SARS-CoV-2 em doentes com Covid-19 durante o curso da doença. Estes achados sugerem que a GM bacteriana humana é afetada pela Covid 19 e pode calibrar a defesa do hospedeiro contra a infeção por SARS-CoV-2.
O microbioma fúngico e a covid-19
O trato GI também alberga um grande número de fungos, coletivamente conhecidos como microbioma (microbioma fúngico), que demonstraram estar implicados de forma causal na montagem e desenvolvimento imunitário da MI [7]. Os doentes com Covid 19 também tinham micobiomas intestinais alterados, caracterizados pelo enriquecimento de Candida albicans e configurações altamente heterogéneas de micobiomas (Figura 1) [8]. A diversidade do micobioma fecal em doentes com Covid 19 na alta foi 2,5 vezes maior do que a dos indivíduos saudáveis. Agentes patogénicos fúngicos oportunistas, Candida albicans, Candida auris e Aspergillus flavus, estavam altamente presentes nas fezes dos doentes com Covid-19 durante o curso da doença. Foram detetados dois agentes patogénicos fúngicos associados a sintomas respiratórios, Aspergillus flavus e Aspergillus niger, em amostras fecais de um subconjunto de doentes com Covid-19, mesmo após a resolução da doença. Micobiomas intestinais instáveis e disbiose prolongada persistiram em aproximadamente 30% dos doentes com Covid-19.
O viroma intestinal e a Covid-19
Através da sequenciação viral do RNA de shotgun, foi encontrada uma assinatura de infeção viral intestinal ativa em 47% dos doentes com Covid-19, mesmo na ausência de sintomas gastrointestinais e após a depuração respiratória do SARS-CoV-2 [9], o que sugere uma infeção “quiescente” por SARS-CoV-2 no trato gastrointestinal e potencial risco de transmissão fecal-oral. Os doentes com tal atividade gastrointestinal do SARS CoV-2 albergaram composições e funções GM anormais, caracterizadas por uma elevada abundância de agentes patogénicos oportunistas e uma maior capacidade de biossíntese de nucleótidos e aminoácidos e metabolismo de hidratos de carbono (glicólise) [9].
O trato GI humano também alberga abundantes membros virais/fágicos coletivamente conhecidos como o viroma intestinal. Os doentes com Covid-19 tinham sub-representação do vírus do mosqueado ligeiro da pimenta (vírus RNA) e múltiplas linhagens de bacteriófagos (vírus DNA) e enriquecimento de vírus DNA eucarióticos derivados do ambiente em amostras fecais, em comparação com indivíduos não-Covid 19 (Figura 1) [10]. O viroma fecal na infeção por SARS-CoV-2 mostrou mais capacidades de codificação genética associada ao stress, inflamação e virulência. Na linha de base do doente, abundância fecal do vírus RNA, vírus da mancha clorótica da pimenta e múltiplas espécies de bacteriófagos mostraram uma correlação inversa com a gravidade da Covid-19. Estes vírus também estiveram inversamente associados a níveis sanguíneos de proteínas pró-inflamatórias, glóbulos brancos e neutrófilos, o que indica que os vírus residentes no intestino poderiam afinar a resposta imunitária do hospedeiro à infeção por SARS-CoV-2. Entre as espécies de vírus DNA associados à gravidade da Covid-19, 40% das espécies mostraram correlação inversa com a idade, o que pode estar subjacente à observação de que os indivíduos idosos correm um risco maior para a Covid-19 manifestamente mais grave.
Conclusão
Em resumo, a recolha de evidência sugere que a MI humana (microbiota bacteriana, micobioma e viroma) é afetada na Covid-19. Tal desregulação persiste mesmo após a resolução da doença, o que constitui potencialmente uma ameaça a longo prazo para a saúde do hospedeiro. A composição da microbiota intestinal está associada às respostas imunitárias do hospedeiro e à gravidade da Covid-19 à infeção por SARSCoV- 2. É necessária mais investigação para explorar os efeitos a longo prazo da Covid-19 e para melhorar a MIdo hospedeiro, e a imunidade desta pandemia viral sem precedentes.









