ДУОДЕНАЛЬНАЯ МИКРОБИОТА У ДЕТЕЙ С НЕДОСТАТОЧНЫМ ПИТАНИЕМ И ЭНТЕРОПАТИЕЙ
РЕЦЕНЗИИ - РАЗДЕЛ, ПОСВЯЩЕННЫЙ ДЕТЯМ
Проф. Эммануэль Мас (Emmanuel Mas)
Отделение гастроэнтерологии и нутрициологии, Детская больница, Тулуза, Франция
Раздел для широкой публики
Найдите здесь свое выделенное место
en_sources_title
en_sources_text_start en_sources_text_end
Делиться - значит заботиться
Возможно, эта тема заинтересует ваших коллег. Почему бы не поделиться ею?
Разделы
Об этой статье
Комментарии к оригинальной статье Chen et al. (N Engl J Med 2020)
Экзогенная дисфункция кишечника (ЭДК) — это загадочное заболевание тонкой кишки, которое предположительно играет роль в недостаточном питании у детей, что, в свою очередь, является актуальной проблемой мирового здравоохранения. Определение частоты данного расстройства затруднено из-за сложности прямого взятия образцов слизистой оболочки тонкой кишки и микробиоты. В этом исследовании участвовали 110 младенцев с линейной задержкой роста, которые жили в городских трущобах в Республике Бангладеш и не получали пользы от нутрициологического вмешательства. Авторы выполнили эндоскопию 80 детям, у которых имела место подтвержденная биопсией ЭДК и были доступны образцы плазмы и двенадцатиперстной кишки. При анализе штаммов бактерий, полученных у детей, обнаружено, что абсолютные уровни общей группы из 14 таксонов, обычно не классифицируемых как энтеропатогены, отрицательно коррелировали с линейным ростом и положительно коррелировали с белками двенадцатиперстной кишки, участвующими в иммуно-воспалительных реакциях. Представительство этих 14 таксонов двенадцатиперстной кишки в фекальной микробиоте значимо отличалось от представительства в образцах, полученных у здоровых детей. У мышей-гнотобиотов, у которых выполняли колонизацию культивированными штаммами бактерий двенадцатиперстной кишки, полученными у детей с ЭДК, развилась энтеропатия тонкой кишки.
Полученные результаты подтверждают существование связи между задержкой роста и компонентами микробиоты тонкой кишки с энтеропатией и дают обоснование для разработки вариантов лечения, направленных на этот микробный вклад в ЭДК.
ЧТО МЫ УЖЕ ЗНАЕМ?
Частота хронического недостаточного питания с задержкой роста составляет 25% среди младенцев с более чем 5 эпизодами диареи. Эти рецидивирующие кишечные инфекции приводят к ЭДК, которая характеризуется атрофией ворсинок, сочетающей уменьшение площади поверхности кишечника и ослабление абсорбционной способности, нарушение кишечного барьера и воспаление слизистой оболочки.
Более свежие данные позволяют предполагать, что при ЭДК может присутствовать дисбиоз микробиоты верхних отделов желудочно-кишечного тракта.
ЧТО ГЛАВНОЕ В ЭТОМ ИССЛЕДОВАНИИ?
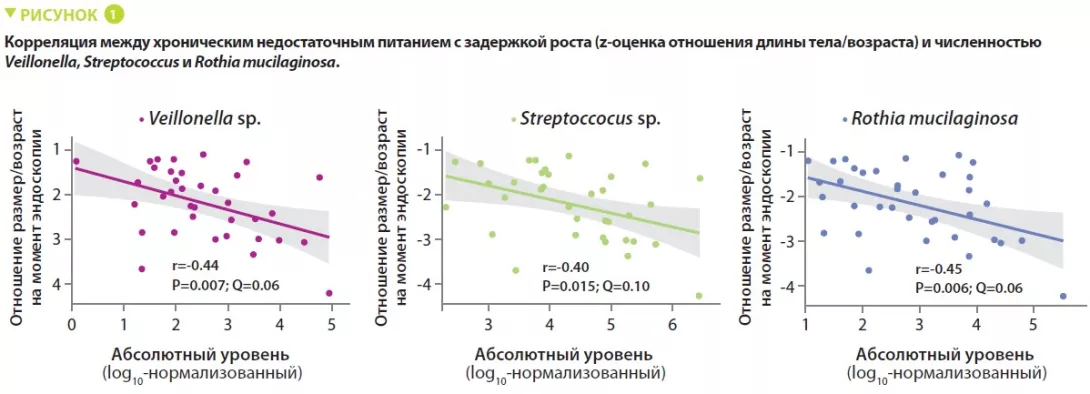
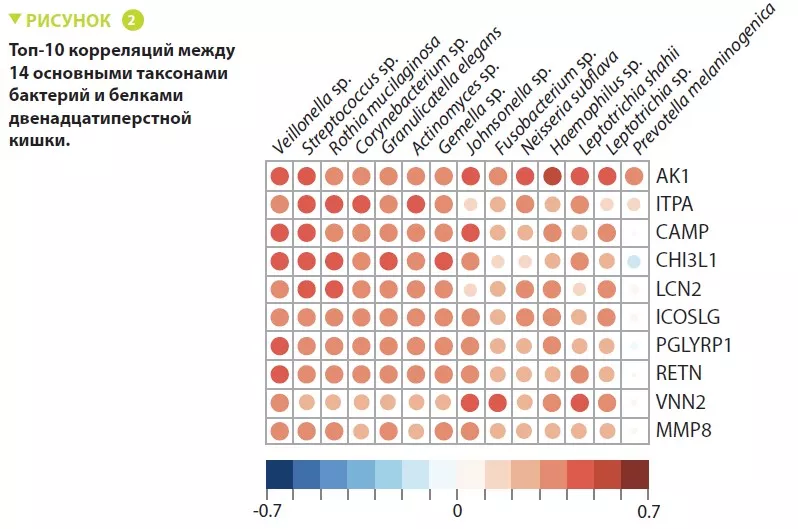
В это исследование включены 110 младенцев в возрасте в среднем 18 месяцев из Дакки (Бангладеш), которые страдали хроническим недостаточным питанием с задержкой роста, определяемым нутрициологическим вмешательством. Биопсия двенадцатиперстной кишки подтвердила наличие ЭДК у 80 из них. Была проанализирована микробиота дуоденального аспирата 36 из этих младенцев; группа из 14 бактериальных таксонов присутствовала более чем у 80% популяции и отрицательно коррелировала с отношением длина тела/возраст (r = - 0,049, p = 0,003) (рисунок 1). Протеомное исследование биоптатов двенадцатиперстной кишки показало положительную корреляцию между этими 14 таксонами и 10 белками, включая 2 противомикробных пептида, и маркером воспаления кишечника (LCN2). Также обнаружена отрицательная корреляция с 10 белками, продуцируемыми энтероцитами (рисунок 2).
У 80 младенцев с ЭДК исследование протеомики плазмы обнаружило сильную положительную корреляцию с REG3A и LCN2.
Сравнение микробиоты кала младенцев с ЭДК и 27 контрольных младенцев выявило значительное увеличение численности бактерий рода Veillonella, которые сильнее всего коррелировали с белками двенадцатиперстной кишки, участвующими в воспалении желудочно-кишечного тракта.
После культивирования 39 штаммов бактерий двенадцатиперстной кишки младенцев с экзогенной дисфункцией кишечника, включая 11 из 14 таксонов, их вводили через желудочный зонд мышам, которые находились на диете, аналогичной диете 18-месячного младенца из Дакки.
Обнаружено, что двадцать три вида из этой группы бактерий присутствовали по меньшей мере в одной части кишечника в относительном количестве >0,1%. Контрольные мыши получали через желудочный зонд микробиоту слепой кишки мышей, выращенных традиционным способом. В отличие от контрольных мышей, у мышей, получавших бактерии, связанные с «экзогенной дисфункцией кишечника», наблюдалась инфильтрация собственной пластинки тонкой кишки воспалительными мононуклеарами в дополнение к аномалиям и деформациям архитектоники эпителия с удлинением крипт. Аномалии имели очаговую локализацию в тонкой кишке, но не распространялись на толстую кишку. С функциональной точки зрения, у этих мышей обнаружено увеличение экспрессии мРНК противомикробных пептидов (Reg3β и Reg3γ), повышение уровня металлопротеиназы (MMP8) и снижение активности мРНК, кодирующей белки плотных контактов.
Эти изменения врожденного иммунного ответа и эпителиального барьера слизистой оболочки могут объяснить системную бактериальную транслокацию в селезенку (Escherichia coli и Enteroccocus hirae).
КАКОВЫ ПРАКТИЧЕСКИЕ ПОСЛЕДСТВИЯ?
Это исследование показывает полезность эндоскопии верхних отделов желудочно-кишечного тракта с биопсией в подтверждении экзогенной дисфункции кишечника.
Тем не менее рекомендовать конкретное терапевтическое лечение пока не представляется возможным.
КЛЮЧЕВЫЕ МОМЕНТЫ
-
Нарушение кишечной микробиоты на уровне двенадцатиперстной кишки способствует экзогенной дисфункции кишечника
-
Этот дисбиоз значительно коррелирует с хроническим недостаточным питанием
-
Патология поддается передаче мышам, что может помочь понять задействованные в ее развитии патофизиологические механизмы (воспаление кишечника, аномалии эпителиального барьера и иммунные изменения бактериальной передачи сигналов)
ЗАКЛЮЧЕНИЕ
Результаты этого исследования предполагают причинно-следственную связь между бактериями двенадцатиперстной кишки, экзогенной дисфункцией кишечника и хроническим недостаточным питанием с задержкой роста. Вероятно, детям с таким заболеванием может помочь разработка методов лечения выявленного дисбиоза.