A colestase altera o desenvolvimento da microbiota intestinal e a atividade da hidrolase dos ácidos biliares em recém-nascidos prematuros
ARTIGO COMENTADO - Rubrica pediátrica
Pelo Prof. Emmanuel Mas
Gastroenterologia e Nutrição, Hospital Saint-Antoine, Paris, França
Área para o público geral
Encontre aqui o seu espaço dedicado
en_sources_title
en_sources_text_start en_sources_text_end
Capítulos

Sobre este artigo
Comentário ao artigo original de Lynch LE et al (Gut Microbes) [1]
A colestase é uma perturbação do fluxo de bílis do fígado para o intestino. Nos recém-nascidos, a colestase leva a um crescimento deficiente e pode progredir para insuficiência hepática e morte. O fluxo normal de bílis requer um eixo fígado-intestino-microbiota intacto, no qual os ácidos biliares primários derivados do fígado são transformados em ácidos biliares secundários. As enzimas microbianas (hidrolase dos ácidos biliares [BSH]) são responsáveis pelo primeiro passo, que consiste na desconjugação dos ácidos biliares primários conjugados com glicina e taurina. Os recém-nascidos colestáticos são frequentemente tratados com ácido ursodesoxicólico (UDCA), um potente ácido biliar colerético, embora as interações entre o UDCA, as bactérias intestinais e outros ácidos biliares sejam pouco conhecidas. Este estudo, baseado em 124 amostras de fezes de 24 recém-nascidos, revelou novas associações que ligam os ácidos biliares isoméricos e a atividade da BSH às trajetórias de crescimento neonatal. Estes dados realçam o facto de a desconjugação dos ácidos biliares ser uma função microbiana essencial, adquirida precocemente no desenvolvimento neonatal e prejudicada pela colestase.
O que é que já sabemos sobre isto?
Os recém-nascidos prematuros, nascidos antes das 37 semanas de amenorreia (SA), correm um maior risco de desenvolver colestase. A colestase, definida como uma redução do fluxo biliar, é favorecida por vários fatores de risco, como a prematuridade, o baixo peso à nascença e a nutrição parentérica. Na ausência de uma etiologia, a condição é conhecida como colestase neonatal transitória. Para melhorar a colestase, é frequentemente efetuado um tratamento com ácido ursodeoxicólico (UDCA). Os ácidos biliares são necessários para a absorção dos lípidos e das vitaminas lipossolúveis. Durante a colestase, verifica-se uma redução da quantidade de ácidos biliares no intestino e uma alteração das proporções dos diferentes ácidos biliares. Os ácidos biliares primários são produzidos a partir do colesterol e conjugados no fígado. Interagem extensivamente com a microbiota intestinal, levando à formação de ácidos biliares secundários através de uma enzima microbiana, a hidrolase dos ácidos biliares (BSH).
Os ácidos biliares e a microbiota intestinal têm um impacto no crescimento e desenvolvimento dos bebés prematuros. Os autores quiseram estudar o impacto da colestase no estabelecimento da microbiota intestinal em bebés muito prematuros e na desconjugação dos ácidos biliares.
Quais são as principais conclusões deste estudo?
Os autores incluíram 24 recém-nascidos pré-termo, 12 colestáticos e 12 controlos, nascidos com 27,2± 1,8 SA, com um peso médio à nascença de 946± 249,6 g. O pico médio de bilirrubina conjugada foi de 7,0 mg/dL. Não se registaram diferenças entre os dois grupos em termos de ambiente intrauterino, modo de parto ou utilização de antibióticos ao longo do tempo.
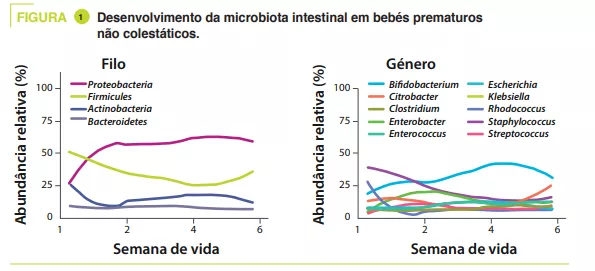
As fezes foram recolhidas desde o nascimento até às seis semanas de idade. A sequenciação (método shotgun) mostrou que a diversidade alfa aumentou nos controlos durante o primeiro mês de vida. Em termos de filos, Proteobacteria e Firmicutes foram os mais abundantes; em termos de géneros, Staphylococcus foi o mais abundante à nascença e depois diminuiu, enquanto a abundância de Klebsiella aumentou gradualmente (figura 1). Clostridium perfringens foi a espécie cuja abundância relativa mais aumentou ao longo do tempo, o que foi definido pela idade pós-menstrual (PMA, soma da idade a termo (SA) e idade pós-natal) (p = 0,01). A análise metagenómica mostrou que a via metabólica mais enriquecida nas fezes maduras (32-40 semanas PMA) em comparação com as fezes menos maduras (25-28 semanas PMA) foi a da biossíntese de ácidos biliares secundários.
Nos controlos, a análise de componentes principais mostrou que o principal fator que influenciava a composição da microbiota intestinal era a PMA, ao passo que não tinha qualquer efeito nos bebés prematuros colestáticos. A via biossintética secundária dos ácidos biliares foi mais enriquecida nas fezes dos controlos do que nos prematuros colestáticos às 32-40 semanas de PMA (p = 0,04). Da mesma forma, os autores encontraram uma diminuição de 55% na abundância relativa do gene BSH (p = 0,04) e Clostridium perfringens (p = 0,0008) em recém-nascidos colestáticos (figura 2).
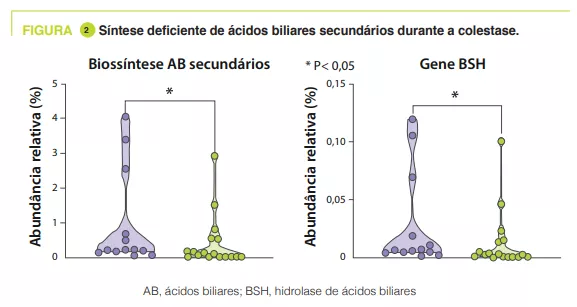
O perfil de ácidos biliares fecais medido por espetrometria de massa mostrou que a proporção de ácidos biliares não conjugados aumentou de 4% às 25-28 semanas PMA para 98% às 32-40 semanas PMA nos controlos, mas para apenas 46% nos doentes colestáticos. É de notar que certos isómeros podem ter um valor preditivo porque aumentam antes do início da colestase.
O UDCA, utilizado em cinco dos 12 bebés prematuros, foi encontrado nas suas fezes numa concentração 522 vezes superior à dos outros sete bebés que não foram tratados. O UDCA modificou a microbiota intestinal com um aumento relativo das Firmicutes e uma diminuição das Proteobacteria (p < 0,05), e ao nível das espécies com um enriquecimento do Clostridium perfringens.
Finalmente, os bebés pré-termo com uma abundância fecal do gene BSH > 0,005% às 32-40 semanas PMA tiveram um aumento de 1,2 vezes nas taxas de crescimento da estatura e de peso em comparação com aqueles com uma abundância < 0,005%. Da mesma forma, uma quantidade de ácido cólico fecal > 30% mostrou um aumento médio nas taxas de crescimento em altura (14%), peso (18%) e perímetro cefálico (15,8%) (p < 0,05).
Quais são as consequências práticas ?
Este estudo permite uma melhor compreensão dos mecanismos fisiopatológicos envolvidos na colestase na desregulação do eixo fígado-intestino-microbiota intestinal. Isto poderia levar à possibilidade de corrigir o ciclo entero-hepático utilizando certos probióticos ou outros medicamentos (com base na atividade do BSH) ou outros medicamentos.
CONCLUSÃO
Nos recém-nascidos extremamente prematuros, a colestase altera o desenvolvimento da microbiota intestinal, reduzindo a aquisição de Clostridium perfringens e a capacidade de síntese de ácidos biliares secundários. Inversamente, um aumento de certos ácidos biliares, ligado à atividade da BSH, está associado a um melhor crescimento neonatal.

