La cholestase altère le développement du microbiote intestinal et l’activité hydrolase des acides biliaires chez des nouveau-nés prématurés
ARTICLE COMMENTÉ - Rubrique enfant
Par le Pr Emmanuel Mas
Gastro-entérologie et nutrition, Hôpital des Enfants, Toulouse, France
Section grand public
Retrouvez ici votre espace dédié
en_sources_title
en_sources_text_start en_sources_text_end
Chapitres

A propos de cet article
Commentaire de l’article original de Lynch LE et al. Gut Microbes [1]
La cholestase est un trouble de l’écoulement de la bile du foie vers l’intestin. Chez les nouveau-nés, la cholestase entraîne une mauvaise croissance et peut évoluer vers une insuffisance hépatique et la mort. Un flux biliaire normal nécessite un axe foie-intestinmicrobiote intact, dans lequel les acides biliaires primaires dérivés du foie sont transformés en acides biliaires secondaires. Les enzymes microbiennes (hydrolase des acides biliaires [BSH]) sont responsables de la première étape, qui consiste à déconjuguer les acides biliaires primaires conjugués à la glycine et à la taurine. Les nouveau-nés cholestatiques sont souvent traités avec l’acide ursodésoxycholique (UDCA), un puissant acide biliaire cholérétique, bien que les interactions entre l’UDCA, les bactéries intestinales et les autres acides biliaires soient mal comprises. Cette étude, portant sur 124 échantillons de selles provenant de 24 nouveau-nés, met en évidence de nouvelles associations liant les acides biliaires isomériques et l’activité BSH aux trajectoires de croissance néonatale. Ces données soulignent le fait que la déconjugaison des acides biliaires est une fonction microbienne essentielle, acquise au début du développement néonatal et altérée par la cholestase.
Que sait-on déjà à ce sujet ?
Les nouveau-nés prématurés, nés avant 37 semaines d’aménorrhée (SA), ont un risque plus important de développer une cholestase. La cholestase, définie par une diminution du flux biliaire, est favorisée par différents facteurs de risque comme la prématurité, un petit poids de naissance et la nutrition parentérale. En l’absence d’étiologie, on parle de cholestase néonatale transitoire. Pour améliorer la cholestase, un traitement par acide ursodésoxycholique (UDCA) est souvent entrepris.
Les acides biliaires sont nécessaires à l’absorption des lipides et des vitamines liposolubles. Lors d’une cholestase, il y a une diminution de la quantité d’acides biliaires au niveau de l’intestin mais également une modification des proportions des différents acides biliaires. En effet, les acides biliaires primaires sont produits à partir du cholestérol et conjugués dans le foie. Leurs interactions avec le microbiote intestinal sont importantes aboutissant à la formation d’acides biliaires secondaires, par l’intermédiaire d’une enzyme microbienne, l’hydrolase des acides biliaires (BSH).
Les acides biliaires et le microbiote intestinal ont un impact sur la croissance et le développement des prématurés. Les auteurs ont voulu étudier le retentissement de la cholestase sur la mise en place du microbiote intestinal chez des grands prématurés et sur la déconjugaison des acides biliaires.
Quels sont les principaux résultats apportés par cette étude ?
Les auteurs ont inclus 24 nouveau-nés prématurés, 12 cholestatiques et 12 témoins, nés à 27,2 ± 1,8 SA, avec un poids de naissance moyen de 946 ± 249,6 g. Le pic moyen de bilirubine conjuguée était de 7,0 mg/dL. Il n’y avait pas de différences entre les deux groupes entre l’environnement intra-utérin, le mode d’accouchement et l’utilisation d’antibiotiques au cours du temps.
Des selles ont été recueillies de la naissance à six semaines de vie. Leur séquençage (méthode shotgun) a montré chez les témoins que l’alpha-diversité augmentait au cours du premier mois de vie. Au niveau des phyla, les Proteobacteria et Firmicutes étaient les plus abondants ; au niveau des genres, Staphylococcus était le plus abondant à la naissance puis diminuait alors que l’abondance de Klebsiella augmentait progressivement (figure 1). Clostridium perfringens était l’espèce dont l’abondance relative augmentait le plus au cours du temps, qui était défini par l’âge post-menstruel (PMA, somme de l’âge au terme de naissance (SA) et de l’âge post-natal) (p = 0,01). L’analyse métagénomique a montré que la voie métabolique qui était la plus enrichie dans les selles matures (32-40 semaines PMA) par rapport aux moins matures (25- 28 semaines PMA) était celle de la biosynthèse des acides biliaires secondaires.
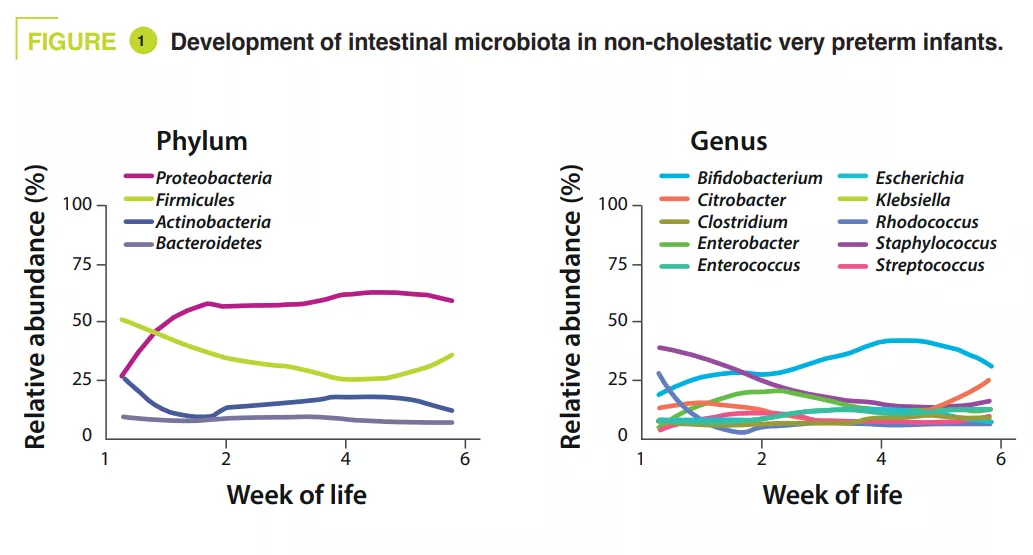
Chez les témoins, l’analyse en composante principale a montré que le principal facteur influençant la composition du microbiote intestinal est le PMA, alors qu’il n’a pas d’effet chez les prématurés cholestatiques. La voie de biosynthèse des acides biliaires secondaires est la plus enrichie dans les selles de témoins vs cholestatiques à 32-40 semaines PMA (p = 0,04). De même, les auteurs ont retrouvé une diminution de 55 % de l’abondance relative du gène BSH (p = 0,04) et de Clostridium perfringens (p = 0,0008) chez les nouveau-nés cholestatiques (figure 2).
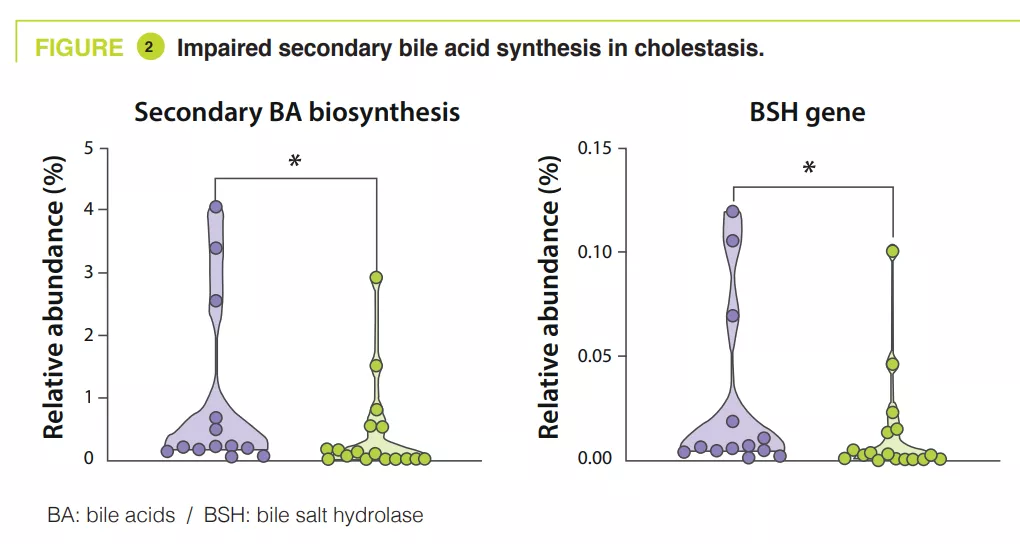
Le profil des acides biliaires fécaux mesuré par spectrométrie de masse a montré que la proportion d’acides biliaires non conjugués augmentait de 4 % à 25-28 semaines PMA à 98 % à 32-40 semaines PMA chez les témoins, mais à seulement 46 % chez les cholestatiques. À noter que certains isomères pourraient avoir une valeur prédictive car ils augmentaient avant le début de la cholestase.
L’UDCA, utilisé chez cinq des 12 prématurés, est retrouvé dans leurs selles à une concentration 522 fois supérieure aux 7 autres non traités. L’UDCA modifiait le microbiote intestinal avec une augmentation relative des Firmicutes et une diminution des Proteobacteria (p < 0,05), et au niveau des espèces avec un enrichissement en Clostridium perfringens.
Enfin, les prématurés avec une abondance fécale du gène BSH > 0,005 % à 32-40 semaines PMA avaient des vitesses de croissance staturale et pondérale augmentées d’un facteur 1,2 en comparaison à ceux qui avaient une abondance < 0,005 %. De même, une quantité d’acide cholique fécal > 30 % montrait une augmentation moyenne des vitesses de croissance de la taille (14 %), du poids (18 %) et du périmètre crânien (15,8 %) (p < 0,05).
Quelles sont les conséquences en pratique ?
Cette étude permet de mieux comprendre les mécanismes physiopathologiques impliqués lors de la cholestase dans la dérégulation de l’axe foie-intestin-microbiote intestinal. Cela permettrait d’envisager une correction du cycle entéro-hépatique à l’aide de certains probiotiques ou autres médicaments (basés sur l’activité de la BSH) ou autres médicaments
CONCLUSION
Chez les nouveau-nés grands prématurés, la cholestase modifie la mise en place du microbiote intestinal, en diminuant l’acquisition de Clostridium perfringens et la capacité de synthèse des acides biliaires secondaires. À l’inverse, une augmentation de certains acides biliaires, en lien avec l’activité de la BSH, est associée à une meilleure croissance néonatale.

