O intestino da criança no cerne da imunidade
Por Dr Travis J. De Wolfe
Área para o público geral
Encontre aqui o seu espaço dedicado
en_sources_title
en_sources_text_start en_sources_text_end
Capítulos
Sobre este artigo
Autores
Sumário
Sumário
Desenvolvimento de barreiras imunitarias inatas
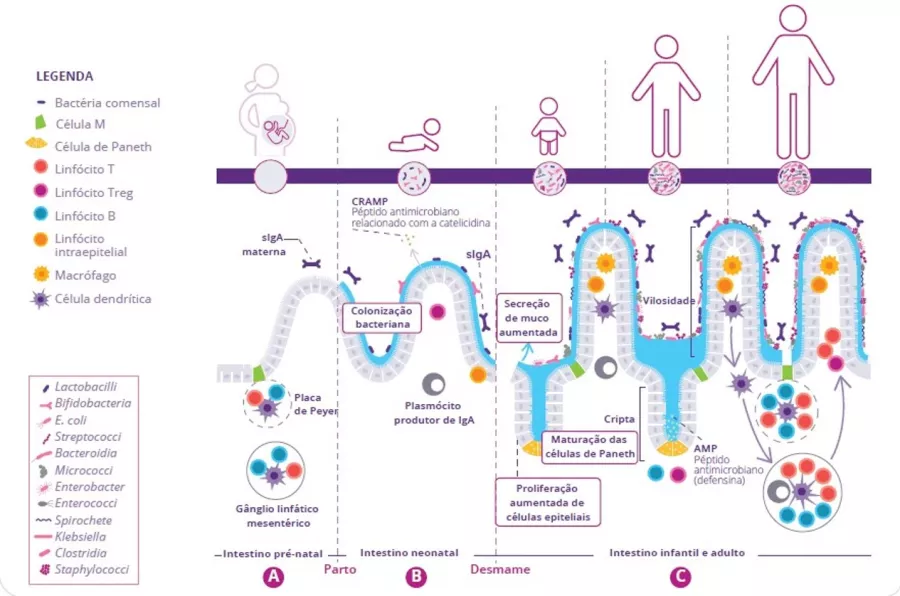
O desenvolvimento do sistema imunitário intestinal começa antes do nascimento e continua até ao desmame neonatal. In utero, são geradas estruturas linfoides imaturas, incluindo placas de Peyer e gânglios linfáticos mesentéricos (figura 1A).
Uma vez que essas estruturas não se encontram inteiramente funcionais até mais tarde no desenvolvimento, para compensar, são produzidos peptídeos antimicrobianos (AMP) pelo epitélio intestinal que funcionam como uma barreira de defesa face aos primeiros colonizadores bacterianos (figura 1B).1 O muco é outra importante estrutura de barreira, produzida pelas células caliciformes e segregada na superfície apical do trato GI. Juntas, estas barreiras imunitárias inatas desempenham um papel fundamental na limitação do contacto direto da microbiota intestinal com as células epiteliais do hospedeiro, especialmente enquanto a microbiota se estabelece no intestino da criança.
80% Pelo menos 80% das células produtoras de Ig do corpo estão localizadas no intestino.
O sistema imunitário adaptativo neonatal também é fundamental durante o desenvolvimento
A imunoglobulina A (IgA) é produzida com afinidade variável relativamente aos componentes da microbiota, bem como a antigénios alimentares específicos ingeridos pelo recém-nascido. A IgA segregada atua para fixar esses alvos no lúmen intestinal e limitar a sua capacidade de aderir e/ou penetrar no epitélio intestinal (figura 1B).2 Paralelamente, durante o desmame, a microbiota intestinal neonatal torna-se cada vez mais diversificada e concentrada em resposta à modificação da dieta e ao desenvolvimento da arquitetura cripto-vilosa. Tal requer proteção adicional da barreira epitelial através da maturação das estruturas linfoides locais. As células de Paneth ativadas começam a produzir proteínas de defesa do hospedeiro (defensinas) na base das criptas do intestino delgado, permitindo que outras células epiteliais deixem de produzir AMP na linha de base. Por fim, a proliferação de células epiteliais aumenta juntamente com o aumento da secreção de muco (figura 1C).
FIGURA 1: Desenvolvimento da microbiota intestinal e do sistema imunitário intestinal antes do nascimento (A), antes do desmame (B) e depois do desmame (C).
Adaptado de Brandtzaeg P, 20173 and Ximenez C et al, 20176
A importancia da homeostase intestinal
Pelo menos 80% das células produtoras de Ig do corpo estão localizadas no intestino:3 este é o maior órgão efetor da imunidade humoral. As células epiteliais especializadas na captura e transporte de antigénios (células M) têm uma função de controlo, facilitando o transporte de antigénios – provenientes de bactérias comensais, da dieta ou de agentes patogénicos – do lúmen intestinal para as células linfoides subjacentes. Esses antigénios serão depois digeridos pelas células dendríticas (DC) e apresentados ao sistema imunitário adaptativo.
Conjuntamente, os diferentes elementos da imunidade intestinal promovem a homeostase através de duas estratégias anti-inflamatórias (figura 1C):
1) A exclusão imunitária de antigénios estranhos limita/evita que a microbiota intestinal colonize ou penetre na mucosa intestinal. Isto é realizado pela sIgA.3
2) 2) A tolerância oral atua para limitar as respostas imunitárias locais e periféricas a antigénios inócuos que entrem em contato com a barreira epitelial.4 Isto depende de células Treg com funções regulatórias (figura 2).3
Quando essas estratégias funcionam de forma adequada, a regulação do sistema imunitário juntamente com as ações da microbiota comensal no desenvolvimento e treino deste sistema leva ao estabelecimento de um relação hospedeiro-comensal durável e homeostática que tem implicações a longo prazo para a saúde humana.5
Para além das células imunitárias: a importância da barreira de muco intestinal
por Dra. Larissa Celiberto
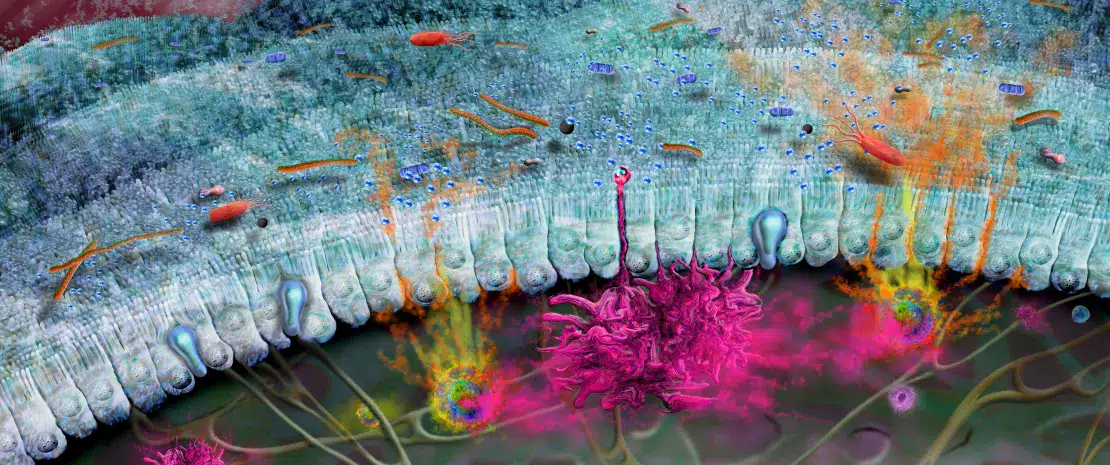
Os intestinos são revestidos por uma camada única de células, chamada epitélio
intestinal, sobre a qual se encontra uma densa camada de muco (figura 1). Juntas, essas
barreiras confinam os micróbios no interior do lúmen intestinal, além de protegerem
o sistema imunitário subjacente de ativação desnecessária pela microbiota.3 O muco
intestinal gera e liberta a mucina 2 (MUC2), uma glicoproteína revestida de açúcar que
proporciona estrutura ao muco. Estudos recentes têm demonstrado que a maturação
e a função da camada de muco são fortemente influenciadas pela microbiota
intestinal, enquanto os tipos de açúcares encontrados na MUC2 também podem
influenciar quais as bactérias que são capazes de se ligar a ela ou de usá-la, e às
suas cadeias de açúcares, como fonte de nutrientes.7 Nomeadamente, uma barreira
de muco perturbada ou incapacitada pode levar a um aumento da penetração ou
da passagem de bactérias potencialmente prejudiciais para fora do lúmen (por
exemplo, intestino permeável), resultando em infeção e inflamação sistémica.8 Além
disso, uma camada de muco defeituosa e a correspondente disbiose da microbiota
intestinal9 observa-se em várias doenças (como a doença inflamatória intestinal (DII),10,11
a diabetes,12 etc.), destacando assim a importância desta barreira protetora para a
saúde humana.
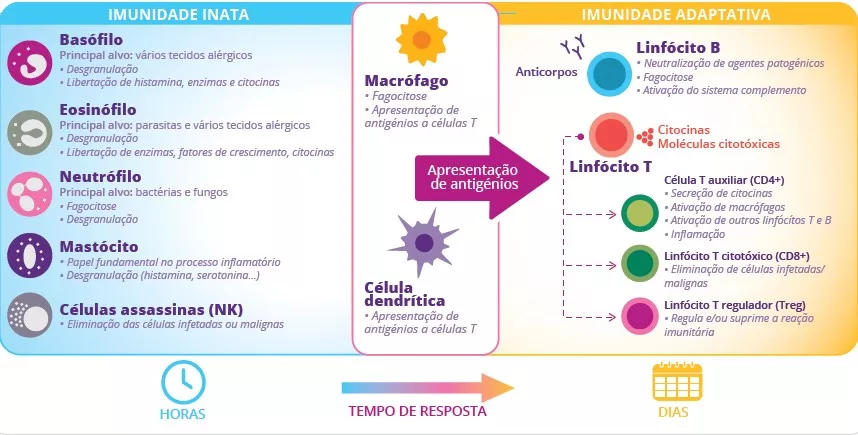
FIGURA 2: Células dos sistemas imunitários inato e adaptativo e respetivas funções.
3 Brandtzaeg P. (2017) Role of the Intestinal Immune System in Health. In: Baumgart D. (eds) Crohn's Disease and Ulcerative Colitis. Springer, Cham.
4 Commins SP. Mechanisms of Oral Tolerance. Pediatr Clin North Am. 2015 Dec;62(6):1523-9.