РАННЕЕ ИСКУССТВЕННОЕ ВСКАРМЛИВАНИЕ СВЯЗАНО С ИЗМЕНЕНИЯМИ МИКРОБИОТЫ КИШЕЧНИКА И ПОВЫШЕННОЙ АНТИБИОТИКОРЕЗИСТЕНТНОСТЬЮ У МЛАДЕНЦЕВ
КОММЕНТАРИИ К СТАТЬЕ - РАЗДЕЛ, ПОСВЯЩЕННЫЙ ДЕТЯМ
Проф. Эммануэль Мас (Emmanuel Mas)
Отделение гастроэнтерологии и нутрициологии, Детская больница, Тулуза, Франция
Раздел для широкой публики
Найдите здесь свое выделенное место
en_sources_title
en_sources_text_start en_sources_text_end
Делиться - значит заботиться
Возможно, эта тема заинтересует ваших коллег. Почему бы не поделиться ею?
Разделы

Об этой статье
Комментарии к статье Pärnänen KMM et al. Am J Clin Nutr 2021 [1]
Младенцы подвержены высокому риску заражения смертельно опасными инфекциями, успех лечения которых зависит от эффективности антибиотиков. Гены антибиотикорезистентности (ARG) присутствуют в большом количестве в кишечной микробиоте младенцев, ранее не получавших антибиотики, а младенческая смертность, вызванная резистентными инфекциями, продолжает оставаться высокой.
Авторы статьи попытались определить влияние раннего искусственного вскармливания на нагрузку ARG у доношенных и недоношенных новорожденных и младенцев. Одно из предположений заключалось в том, что диета влияет на микробное сообщество в кишечнике младенцев, а применение молочных смесей увеличивает содержание таксонов, несущих ARG.
Результаты показали, что у детей на искусственном вскармливании наблюдалось более высокое относительное содержание условно-патогенных микроорганизмов, таких как Staphylococcus aureus, S. epidermidis, Klebsiella pneumoniae, K. oxytoca и Clostridioides difficile. В кишечнике таких детей было значительно меньше потенциально полезных бактерий, например бифидобактерий.
Существование корреляции между искусственным вскармливанием и более высокой нагрузкой ARG у младенцев показывает, что врачи должны учитывать режим кормления при назначении антибиотиков в первые месяцы жизни, чтобы свести к минимуму распространение антибиотикорезистентных штаммов кишечных бактерий.
ЧТО МЫ УЖЕ ЗНАЕМ?
Антибиотикорезистентные бактерии — одна из самых частых причин смерти новорожденных. Появлению резистентных бактерий способствует применение антибиотиков, что связано с большим количеством генов резистентности к антибиотикам (ARG), переносимых резистентными или мультирезистентными бактериальными штаммами. Мобильные генетические элементы (MGE) участвуют в передаче ARG между бактериями. Известно, что тип диеты изменяет микробиоту кишечника, а также количество ARG. При этом в литературе содержится совсем немного данных о связи между резистентностью и рационом питания младенцев.
ЧТО ГЛАВНОЕ В ЭТОМ ИССЛЕДОВАНИИ?
Авторы включили в исследование 46 младенцев, родившихся преждевременно в период между 26 и 37 неделями гестации, из которых 21 получал смесь, 20 — обогащенное грудное молоко и 5 — грудное молоко. Образцы кала собирали в течение 36 дней для анализа состава кишечной микробиоты и наличия ARG. 30 детей получали лечение антибиотиками: образцы кала собирали приблизительно через две недели после окончания лечения для минимизации действия вмешивающихся факторов.
Для сравнения информации с литературными данными параллельно анализировали результаты метаанализа пяти исследований, включавших 696 новорожденных с аналогичными характеристиками.
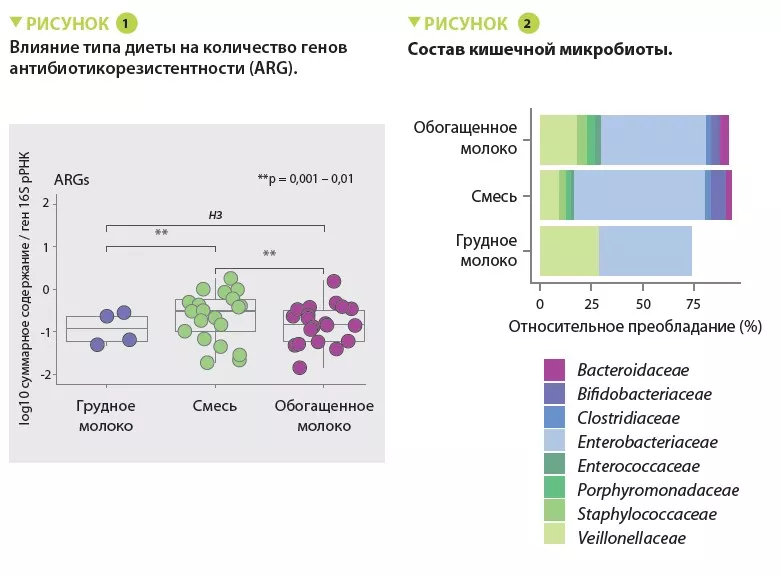
Результаты показали, что у младенцев, получавших смесь, было значимо больше ARG, чем у детей, получавших обогащенное грудное молоко (х 3,6; 95% ДИ, 1,61-8,9) или грудное молоко (х 4,3; 95% ДИ, 1,61-11,56) (p < 0,01) (рисунок 1). Содержание MGE было увеличено аналогичным образом (р < 0,05).
Преобладание Enterobacteriaceae, чей геном содержит больше мобильных ARG, было выше у младенцев, получавших смесь (р < 0,05) (рисунок 2), и, как правило, обратно коррелировало с гестационным возрастом (р < 0,1). Была отмечена обратная корреляция между сроком беременности и содержанием этих ARG (х 0,72; 95% ДИ, 0,57- 0,89) (р < 0,001). Некоторые ARG значимо преобладали у младенцев, получавших смесь, включая гены, кодирующие бета-лактамазы расширенного спектра, присутствующие у Klebsiella (р < 0,05).
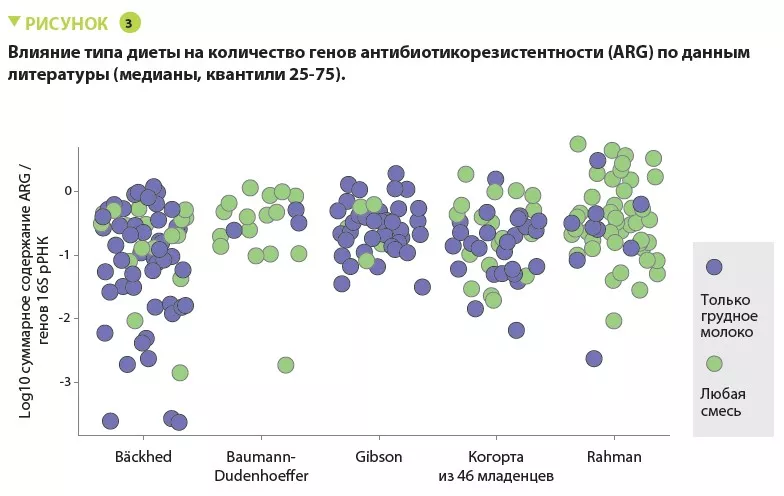
А н а л о г и ч н ы е р е з у л ь т а т ы п о л у ч е н ы и в м е т а а н а л и з е : у н о в о р о ж д е н н ы х , п о л у ч а в ш и х с м е с ь , у с т а н о в л е н о относительное увеличение ARG на 70% (p = 0,013). Медианная нагрузка ARG была выше у младенцев, получавших смесь, во всех когортах (рисунок 3). Наконец, анализ кишечной микробиоты показал у м е н ь ш е н и е п р е о б л а д а н и я б а к т е р и й семейств Bifidobacteriaceae, Veillonellaceae, C l o s t r i d i a c e a e , L a c h n o s p i r a c e a e и Porphyromonadaceae (включая облигатные анаэробные бактерии) у новорожденных, получавших детскую смесь, и увеличение содержания факультативных анаэробных бактерий семейств Enterobacteriaceae, Staphyloccoccaceae и Enterococcaceae ( p < 0 , 0 5 ) . К р о м е т о г о , у э т и х д е т е й о т м е ч а л о с ь у в е л и ч е н и е с о д е р ж а н и я нескольких потенциально патогенных видов, включая факультативные анаэробные микроорганизмы, такие как S. aureus, S. epidermidis, K. pneumoniae, K. oxytoca и о б л и г а т н ы е а н а э р о б н ы е б а к т е р и и Clostridioides difficile (р < 0,001). Таким образом, использование детских смесей повышает содержание патогенных бактерий с ARG в кишечнике.
К А К О В Ы П Р А К Т И Ч Е С К И Е ПОСЛЕДСТВИЯ?
Эти результаты подтверждают пользу г р у д н о г о в с к а р м л и в а н и я . К о р м л е н и е недоношенных новорожденных с помощью смеси ассоциируется с увеличением ARG на 70% по сравнению с детьми, находящимися исключительно на грудном вскармливании. Обогащенное грудное молоко вызывает меньшее увеличение числа ARG.
КЛЮЧЕВЫЕ МОМЕНТЫ
- Использование детских смесей связано с ростом числа генов антибиотикорезистентности (ARG) в микробиоте кишечника.
- Резистентность передаётся между бактериями с помощью мобильных генетических элементов, в основном за счет представителей Enterobacteriaceae, содержание которых повышается у младенцев, получающих смеси.
ЗАКЛЮЧЕНИЕ
Помимо рационального использования антибиотиков, у недоношенных новорожденных важно учитывать тип диеты, отдавая предпочтение грудному молоку во избежание размножения резистентных бактерий.

