Diarreia viral: poderão as vacinas alterar o jogo?
As diarreias virais apresentam-se normalmente como diarreia aquosa e são causadas por 5 tipos principais de vírus. Entre eles, o rotavírus continua a ser a principal causa de mortalidade relacionada com a diarreia nas crianças com menos de 5 anos de idade, apesar da existência de vacinas desde 2006. A composição da microbiota intestinal, implicada nos resultados da infeção viral e na eficácia da vacina contra o rotavírus, pode desempenhar um papel fundamental nas estratégias destinadas a reduzir o impacto da diarreia viral.
Área para o público geral
Encontre aqui o seu espaço dedicado
en_sources_title
en_sources_text_start en_sources_text_end
Capítulos
Sobre este artigo
Rotavírus, norovírus, sapovírus, astrovírus e adenovírus: existem cinco tipos de vírus que são atualmente reconhecidos como as principais causas de diarreia viral.21
Dos mais de 2 mil milhões de episódios de doença diarreica que ocorrem anualmente em todo o mundo, segundo as estimativas do estudo Global Burden of Disease (GBD) de 2016,2 quase 900 milhões dos episódios moderados a graves foram atribuídos a apenas três destes vírus: rotavírus, norovírus e adenovírus.22.
ROTAVÍRUS, PRINCIPAL CAUSA DE MORTE POR DIARREIA NAS CRIANÇAS
Apesar do desenvolvimento e da disponibilização de vacinas contra o rotavírus desde 2006,22 este vírus, que causa sintomas mais graves do que a maioria dos outros agentes patogénicos entéricos,22 foi ainda responsável por mais de 228.000 mortes em todo o mundo em 2016, das quais mais de 128 000 ocorreram em crianças com idade inferior a 5 anos2 – fazendo do rotavírus a principal causa de mortalidade relacionada com a diarreia neste segmento da população (Figura 4).
DIARREIA AQUOSA
Qualquer que seja o vírus que desencadeia um episódio de diarreia, o processo de infeção é basicamente o mesmo: o vírus infecta as células epiteliais do intestino delgado e causa danos que dificultam a absorção de fluidos.21 A diarreia viral manifesta-se geralmente sob a forma de uma diarreia aquosa (sem sangue). Pode ser acompanhada de outros sintomas, nomeadamente náuseas, cólicas abdominais, vómitos e febre22, dando origem ao que se designa por gastroenterite viral.
REIDRATAÇÃO... E PROBIÓTICOS
Tal como para as outras etiologias da diarreia infeciosa (bacterianas ou parasitárias), o tratamento da diarreia viral baseia-se na terapia de reidratação oral ou intravenosa, dependendo do grau de desidratação.21 Além disso, de acordo com as conclusões mais recentes do comité ESPGHAN (2023),20 os profissionais de saúde podem recomendar algumas estirpes probióticas (L. rhamnosus, S. boulardii e L. reuteri) para o tratamento da gastroenterite aguda em crianças, uma vez que existe alguma evidência (certeza da evidência: baixa; grau de recomendação: fraco) de redução da duração da diarreia, do tempo de hospitalização ou do débito fecal.
De entre todos os agentes patogénicos diarreicos, e apesar da existência de vacinas, o rotavírus continua a ser o principal responsável pela morte de crianças com menos de cinco anos de idade. 2
MELHORAR A EFICÁCIA DA VACINA CONTRA O ROTAVÍRUS, UM DESAFIO AINDA POR SUPERAR
No que diz respeito à prevenção, são aplicáveis as medidas preventivas habituais (assegurar água potável, higiene adequada e lavagem frequente das mãos, limitar o contacto com pessoas infetadas, etc.). Dado o impacto considerável da doença diarreica por rotavírus, as vacinas contra o rotavírus são outra medida preventiva importante. 22,23
SARS-COV-2: UM NOVO MEMBRO DO CLUBE DOS VÍRUS DIARREICOS
Juntamente com os vírus há muito reconhecidos como principais causas de diarreia viral, a infeção pelo SARS-CoV-2, responsável pela maior pandemia dos últimos tempos – a COVID-19 – também pode dar origem a diarreia. Nos estudos clínicos, a taxa de incidência de diarreia varia de 2% a 50% dos casos.27 Tal como acontece com o trato respiratório, os recetores da enzima conversora de angiotensina 2 (ACE2) encontram-se fortemente expressos nas células intestinais, servindo como um importante local de entrada do vírus no intestino. Os possíveis mecanismos que levam ao desenvolvimento da diarreia envolvem principalmente desregulações da enzima conversora da angiotensina 2 após a entrada do vírus no enterócito, o que poderá desencadear uma resposta inflamatória, desequilíbrio iónico e aumento da permeabilidade. Além disso, a proteína spike do SARS-CoV-2 funciona como uma enterotoxina, com um mecanismo semelhante ao da enterotoxina NSP4 do rotavírus.28 Pensa-se também que a alteração da microbiota intestinal e os efeitos secundários dos medicamentos (antivíricos e antibióticos) possam estar envolvidos.29

Microbiota: um papel fundamental na eficácia da vacinação contra o rotavírus
Desde a sua introdução em 2006, as vacinas orais contra o rotavírus (ORVV) provocaram, a nível mundial, uma descida significativa do número de hospitalizações e de mortes devidas à diarreia por rotavírus.30 No entanto, a eficácia das vacinas tem sido variável, com os países de baixo nível de rendimentos a registarem um desempenho inferior em comparação com a eficácia notavelmente elevada (>90%) observada nos países de rendimento mais elevado.31 Pensa-se que as razões para esta disparidade são multifatoriais (imunidade do hospedeiro, parâmetros perinatais, genética, estado nutricional, stress, consumo de tabaco e álcool, localização rural versus urbana, dimensão da família, etc.). Tal como acontece com outras vacinas, a composição e a função da microbiota intestinal são consideradas um fator fundamental que regula a resposta imunitária à vacinação30,32,33 (Figura 5).
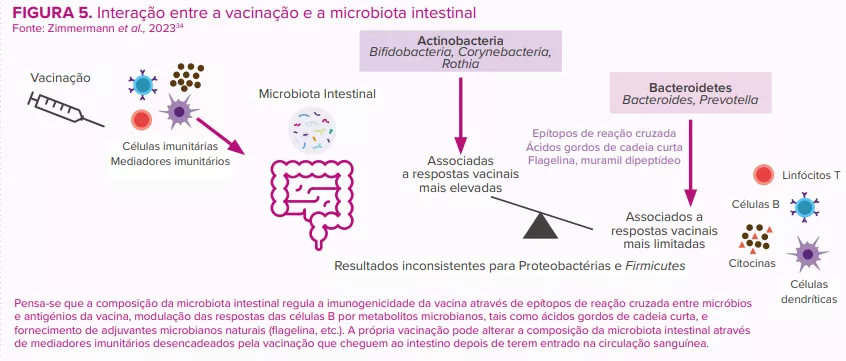
Estima-se que estas vacinas tenham evitado 139 000 mortes por rotavírus em menores de cinco anos durante o período de 2006 a 2019 e que tenham evitado 15% das mortes por rotavírus em menores de cinco anos em 2019.24 No entanto, a eficácia da vacina é específica de cada região e apresenta uma seroconversão fraca nos países de baixo e médio nível de vida. Dados de ensaios clínicos em seres humanos apontam para uma possível ligação entre a microbiota intestinal e a resposta do sistema imunitário entérico à vacina contra o rotavírus25 (Figura 5).
Estima-se que cada grama de conteúdo intestinal humano contenha, pelo menos, 108 a 109 partículas semelhantes a vírus, a grande maioria das quais são fagos.14
MICROBIOTA: ALIADO OU INIMIGO NO INÍCIO DA DIARREIA VIRAL?
Nos casos de diarreia viral, tal como nas diarreias infeciosas em geral, o resultado do confronto entre o agente patogénico e o hospedeiro depende de equilíbrios complexos que envolvem, em grande parte, a microbiota.
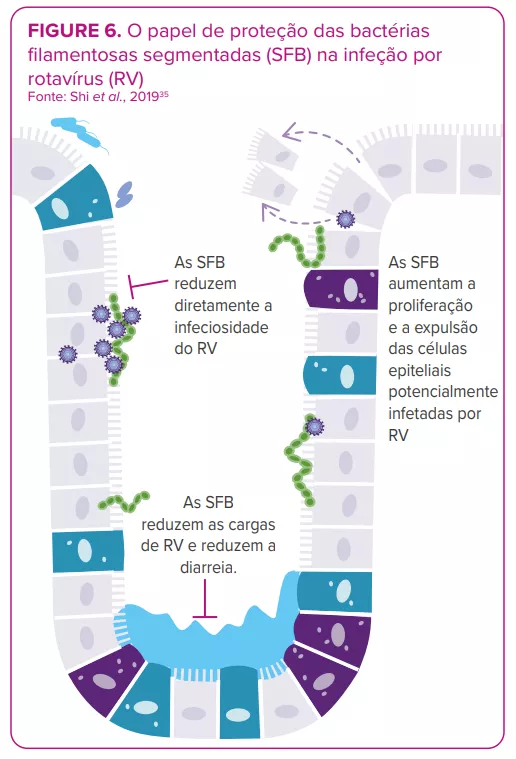
A microbiota intestinal apresenta interações bidirecionais com as infeções por rotavírus e norovírus:14 tanto pode proteger como predispor o hospedeiro à infeção; por sua vez, uma infeção pode alterar a microbiota intestinal. Algumas bactérias parecem ser capazes de inibir a infeção viral. Por exemplo, há um estudo que mostra que as bactérias filamentosas segmentadas previnem e curam a infeção por rotavírus em colónias de ratos35 (Figura 6). Por outro lado, estudos in vitro e in vivo indicam o envolvimento da microbiota intestinal na facilitação da infeção viral: certos micróbios intestinais (por exemplo, Enterobacter cloacae) estimulam a capacidade do norovírus humano para infetar linfócitos B humanos in vitro; a eliminação da microbiota através dos antibióticos atrasa a infeção, reduz a infecciosidade e/ou o título viral do norovírus e do rotavírus em ratos.8,36
Por conseguinte, quaisquer agentes patogénicos invasivos podem ter efeitos diferentes consoante o estado da microbiota intestinal.3 O perfil ideal da microbiota e as melhores estratégias orientadas para a microbiota que possam reduzir o risco de infeção e a diarreia viral que se segue continuam por caraterizar.37
Quanto ao efeito da infeção viral na composição da microbiota intestinal, numerosos estudos documentaram perfis específicos de disbiose em doentes que sofrem de diarreia viral em comparação com controlos saudáveis25,38. É frequentemente relatada uma redução da diversidade (alfa) da microbiota, mas os aumentos ou diminuições de taxa específicos variam muito entre os estudos.14 E permanece uma interrogação: a disbiose observada durante a diarreia viral reflete uma predisposição que pode ter facilitado a infeção, é um estado causado pelo vírus, ou é uma combinação de ambos?
CASO CLÍNICO pelo Dr. Marco Poeta
- Uma menina de 4 anos deu entrada no serviço de urgência pediátrica com febre, diarreia, vómitos e desidratação grave.
- Como a criança precisava de reidratação intravenosa, ficou internada no hospital.
- A zaragatoa nasofaríngea deu positivo para a infeção por SARS-CoV-2, apesar da ausência de sintomas respiratórios.
- As fezes revelaram-se negativas para rotavírus, norovírus, adenovírus, bactérias e parasitas, mas positivas para SARS-CoV-2.
- Após a administração de probióticos, a frequência e a consistência das fezes foram ambas recuperadas.
- A hidratação intravenosa foi interrompida passados quatro dias e a criança recebeu alta.
- A diarreia pode ser a única manifestação clínica da infeção por SARS-CoV-2. O SARSCoV-2 deve, portanto, ser acrescentado à lista de agentes patogénicos entéricos.
- A eficácia dos probióticos contra a gastroenterite associada à Covid observada neste caso clínico está já demonstrada através de estudos in vitro.

OPINIÃO DE ESPECIALISTA
Os probióticos são recomendados como um meio ativo de tratamento da diarreia viral nas crianças, exercendo um efeito antidiarreico que restaura a composição da microbiota a partir do seu estado alterado. Em ensaios clínicos, algumas estirpes probióticas reduzem a diarreia secretora num período de tempo muito curto, mensurável poucas horas após o início da administração de probióticos. Considerando que são normalmente necessários vários dias para se estabelecerem alterações na composição da microbiota, a rápida eficácia dos probióticos pressupõe a existência de efeitos positivos adicionais. As moléculas segregadas pelas bactérias que atuam diretamente nas células intestinais poderão inibir a diarreia secretora através de um mecanismo antioxidante. Este fenómeno é designado o "efeito pósbiótico". Os metabolitos produzidos pelos probióticos têm uma ação semelhante à farmacológica e podem representar terapias inovadoras para o tratamento da diarreia viral.




