ВОССТАНОВЛЕНИЕ МИКРОБИОТЫ КИШЕЧНИКА ПАЦИЕНТОВ, ПОЛУЧАВШИХ АНТИБИОТИКИ, ПУТЕМ АУТОЛОГИЧНОЙ ТРАНСПЛАНТАЦИИ ФЕКАЛЬНОЙ МИКРОБИОТЫ
РЕЦЕНЗИИ - РАЗДЕЛ «ВЗРОСЛЫЕ»
Автор: проф. Гарри Сокол (Harry Sokol)
Gastroenterology and Nutrition Department, Saint-Antoine Hospital, Paris, France
Раздел для широкой публики
Найдите здесь свое выделенное место
en_sources_title
en_sources_text_start en_sources_text_end
Делиться - значит заботиться
Возможно, эта тема заинтересует ваших коллег. Почему бы не поделиться ею?
Разделы

Faecal transplant preparation. A technician storing a prepared sample of human faecal matter in cold storage.
Об этой статье
Автор
Комментарии к оригинальной публикации Таур и соавт. (Science Translational Medicine 2018)
Лечение антибиотиками может истощить популяции комменсальных бактерий микробиоты кишечника пациента и, как это ни парадоксально, повысить риск развития последующих инфекций. При аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК) назначение антибиотиков необходимо для получения оптимальных клинических результатов, но оно значительно нарушает разнообразие микробиоты кишечника, что приводит к потере многих полезных микробов. Хотя отмечена связь снижения разнообразия микробиоты кишечника во время алло-ТГСК с повышенной смертностью, подходы к восстановлению истощенных популяций комменсальных бактерий еще не разработаны. Было инициировано рандомизированное контролируемое клиническое исследование, для того чтобы сравнить аутологичную трансплантацию фекальной микробиоты (ауто-ТФМ) с отсутствием такого вмешательства; были проанализированы профили микробиоты кишечника 25 пациентов с алло-ТГСК (14 пациентам была выполнена ауто-ТФМ, а 11 контрольным пациентом ауто-ТФМ не проводилась). Изменения в разнообразии и составе микробиоты кишечника показали, что благодаря ауто-ТФМ разнообразие микробов увеличилось и восстановился состав микробиоты кишечника, который был у пациента перед лечением антибиотиками и проведением алло-ТГСК. Эти результаты демонстрируют потенциальную пользу сбора образцов кала для проведения ауто- ТФМ с целью последующего восстановления микробиоты кишечника пациента после лечения антибиотиками во время алло-ТГСК, истощающего микробиоту.
ЧТО УЖЕ ИЗВЕСТНО ПО ДАННОЙ ТЕМЕ?
Лечение антибиотиками повреждает микробиоту кишечника и повышает риск возникновения желудочно-кишечной инфекции. Несмотря на то, что этот эффект признавался в течение более 60 лет, восстановление истощенной антибиотиками микробиоты кишечника еще не стало стандартной клинической практикой. Пациентам, перенесшим аллогенную трансплантацию гемопоэтических стволовых клеток (алло-ТГСК), антибиотики обычно назначаются для лече- ния или снижения риска развития серьезной инфекции. Проспективные исследования пациентов с алло-ТГСК показали, что состав микробиоты кишечника заметно изменяется во время лечения, при этом наблюдается значительная потеря облигатных анаэробных бактерий, включая иммуномодулирующие виды бактерий, например класса Clostridia и Bacteroidetes phylum [2]. Клинические последствия этих изменений также очевидны при алло-ТГСК: нарушение баланса полезных облигатных анаэробов коррелирует с осложнениями, которые включают системную инфекцию устойчивыми к ванкомицину штаммами Enterococcus (УВЭ), инфекцию Clostridium difficile и реакцию «трансплантат против хозяина» (РТПХ) [2, 3]. В целом у пациентов, у которых нарушается разнообразие микробиоты кишечника во время приживления гемопоэтических стволовых клеток, наблюдаются более высокие показатели смертности, связанной с трансплантацией [4].
КАКОВЫ ОСНОВНЫЕ РЕЗУЛЬТАТЫ ЭТОГО ИССЛЕДОВАНИЯ?
Пациенты, перенесшие алло-ТГСК, имеют ослабленный иммунитет в течение многих месяцев после приживления, и, несмотря на то, что пациенты с ослабленным иммунитетом, включая реципиентов алло-ТГСК, перенесли гетерологичную ТФМ без по-бочных эффектов [5], авторы пришли к выводу, что аутологичная ТФМ является более безопасной, поскольку сводит к минимуму риск воздействия потенциально патогенных микроорганизмов, ранее не встречавшихся у пациента. Авторы инициировали рандомизированное контролируемое клиническое исследование для определения пригодности ауто-ТФМ для восстановления микробиоты кишечника и уменьшения осложнений, связанных с алло-ТГСК. Здесь они представляют анализ изменения состава микробиоты кишечника у 25 включенных в исследование и рандомизированных пациентов, у которых образцы кала были отобраны в ходе продольного исследования.
Авторы впервые подтвердили в своей группе из 753 пациентов (3237 отобранных образцов кала в ходе продольного исследования), что алло-ТГСК и различные связанные с ними виды антибиотикотерапии вызывали заметное снижение разнообразия микробиоты кишечника, которое достигало самого низкого значения через 5 дней после проведения алло-ТГСК и сохранялось в течение не менее 6 недель, при этом разнообразие микробиоты у большинства пациентов не восстановилось через 100 дней после проведения алло-ТГСК.
ОСНОВНЫЕ ПОЛОЖЕНИЯ
-
Состав микробиоты кишечника заметно нарушается во время аллогенной ТГСК, и это нарушение может играть роль в развитии сопутствующих осложнений
-
Ауто-ТФМ является пригодной и эффективной стратегией восстановления микробиоты после дисбаланса, вызванного аллогенной ТГСК
-
Последствия восстановления микробиоты с точки зрения гематологических показателей еще предстоит оценить
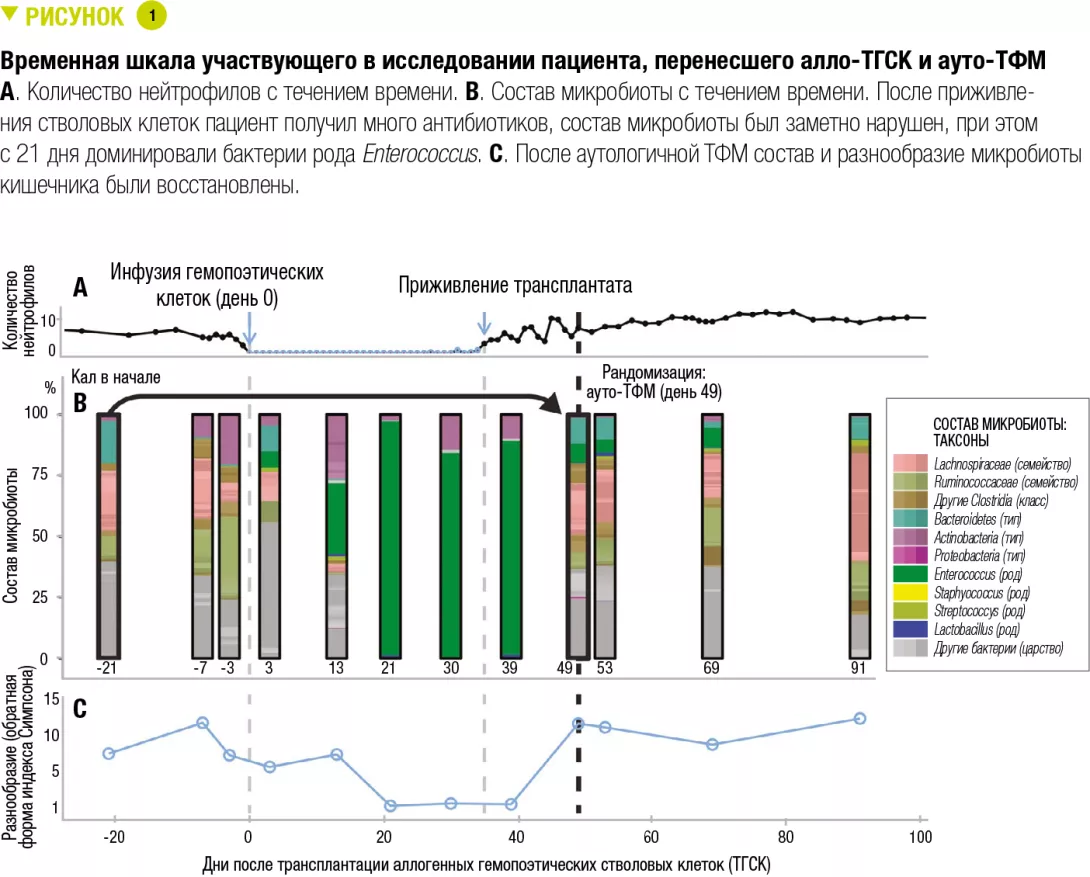
В рамках рандомизированного исследования образцы кала пациентов, отобранные до проведения алло-ТГСК, заморозили при температуре -80 °C и хранили. Через 1–5 недель (в среднем через 13 дней) после алло-ТГСК после приживления (определяемого по восстановлению количества нейтрофилов до > 500/мм3) была выполнена повторная оценка состояния пациентов со взятием кала на анализ. Если бактерии Bacteroidetes были в недостаточном количестве, то пациентов рандомизировали. Представлены результаты анализов микробиоты первых 25 подлежащих оценке пациентов (14 пациентов из группы с ауто-ТФМ и 11 – из контрольной группы). Ауто-ТФМ была выполнена с помощью однократной удерживающей клизмы после подготовки толстой кишки с использованием полиэтиленгликоля аналогично приготовлению для колоноскопии. Авторы демонстрируют, что ауто-ТФМ не только восстанавливает разнообразие микробиоты кишечника, но также и ее состав до проведения алло-ТГСК.
КАКОЕ ПРАКТИЧЕСКОЕ ЗНАЧЕНИЕ ИМЕЮТ ЭТИ РЕЗУЛЬТАТЫ?
Несколько исследований демонстрируют, что микробиота кишечника и ее нарушения играют роль в развитии общих инфекционных и неинфекционных осложнений, встречающихся при проведении алло-ТГСК. Это первое исследование показывает, что отбор и хранение образцов кала пациента перед проведением алло-ТГСК для введения их после приживления являются пригодной и эффективной стратегией восстановления микробиоты. Пока еще неизвестно, наблюдаются ли у пациентов, перенесших ауто-ТФМ, лучшие результаты в отношении этих осложнений и лучшие показатели общей выживаемости. Если эффективность этой стратегии подтверждена, то ее также можно рассматривать в других ситуациях, когда предполагается значительное нарушение состава микробиоты, например в результате лечения антибиотиками широкого спектра действия или дли- тельной антибиотикотерапии или противораковой химиотерапии.
ЗАКЛЮЧЕНИЕ
Несмотря на то, что преимущества с точки зрения гематологических результатов и общей выживаемости еще предстоит оценить, ауто- ТФМ является многообещающей стратегией для восстановления микробиоты кишечника после нарушений, вызванных лечением антибиотиками, связанным с алло- ТГСК.