Un acide gras à chaîne courte du microbiote intestinal pour lutter contre l’endométriose ?
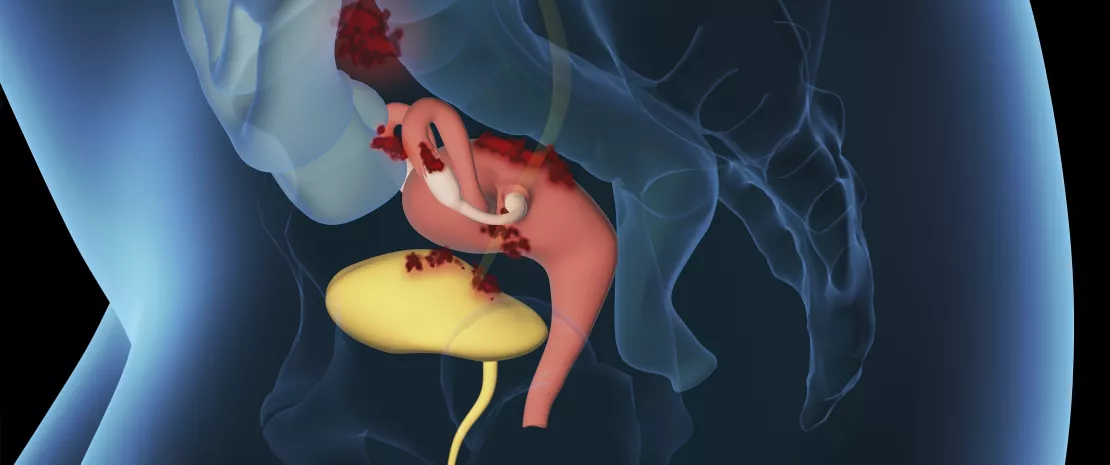
L’endométriose altère considérablement la qualité de vie des femmes atteintes par les douleurs et l’infertilité qu’elle peut entraîner. Alors qu’elle concerne 1 femme sur 10, ses mécanismes restent mal compris et ses traitements, insatisfaisants. Une récente étude1 sur l’animal ouvre de nouvelles perspectives en montrant que le butyrate, un acide gras à chaîne courte produit par le microbiote intestinal, freine le développement des lésions endométriosiques.
Section grand public
Retrouvez ici votre espace dédié
en_sources_title
en_sources_text_start en_sources_text_end
A propos de cet article
Les théories sur l’origine de l’endométriose demeurent non élucidées. Selon l’hypothèse qui prévaut aujourd’hui, des fragments d’endomètre migrent hors de l’utérus dans l’espace péritonéal lors de menstruations rétrogrades et s’implantent sur les tissus environnants. Mais, si 90% des femmes ont des menstruations rétrogrades, seules 10% ont une endométriose. De plus, les traitements actuels de la maladie ne sont pas sans effets secondaires et ne préviennent pas les récidives.
Afin de proposer aux femmes de nouvelles solutions thérapeutiques, d’autres facteurs contribuant à l’altération de l’environnement péritonéal et au développement des lésions doivent être identifiés. Dans ce contexte, le microbiote intestinal suscite l’attention des chercheurs. En effet, celui des femmes atteintes d’endométriose présente une diversité alpha moindre et une composition bactérienne altérée par rapport aux femmes sans endométriose. De plus, les métabolites produits par la flore colique d’un modèle de souris d’endométriose sont différents de ceux des souris contrôle. Ce point est important, car c’est par les métabolites issus de la transformation des fibres alimentaires que le microbiote intestinal apporte ses bénéfices à l’organisme humain. Parmi ceux-ci, les acides gras à chaine courte (AGCC) tels que le butyrate, l’acétate ou le propionate ont notamment des effets antiprolifératifs et anti-inflammatoires. Les auteurs de l’étude publiée dans Life Science Alliance se sont donc penchés sur le rôle de ces AGCC dans l’endométriose in vivo sur un modèle murin d’endométriose et in vitro sur des cellules de lésions endométriosiques.
Le butyrate inhibe la croissance des lésions en activant plusieurs mécanismes
Les premiers résultats montrent que l’endométriose déséquilibre le microbiote intestinal des souris en entraînant une réduction de la production de butyrate. L’équipe observe également que le butyrate (et non d’autres AGCC comme l’acétate ou le propionate) inhibe la croissance des lésions endométriosiques. Le butyrate agirait via au moins trois mécanismes : en activant des récepteurs membranaires couplés aux protéines G (RCPG) : GPR43 et GPR109A, en inhibant l’enzyme histone désacétylase (HDAC) et en activant Rap1GAP (protéine activatrice de GTPase Ras-proximate-1). Rap1GAP bloque la voie de signalisation Rap1 impliquée dans la prolifération, la migration et l’adhésion des cellules. Elle est déjà connue comme un suppresseur de tumeur, y compris dans le cancer de l’endomètre.
De nouvelles études devront désormais déterminer si, chez les femmes atteintes d’endométriose, le taux de butyrate fécal est plus bas que chez les femmes non atteintes. Si tel est le cas, différentes approches destinées à prévenir le développement des lésions pourraient être testées : régime alimentaire, analogues du butyrate, compléments à base de butyrate ou probiotiques induisant la production de butyrate.
Recommandé par notre communauté

"Merci pour cet article !" - Commentaire traduit de Diome🌺 (Repris de Biocodex Microbiota Institute sur X)