Les troubles fonctionnels intestinaux : un ensemble défini en lien avec le microbiote intestinal
Le microbiote intestinal, facteur étiologique et voie de réponse thérapeutique des TFI ? Les deux hypothèses se confirment et se complètent au fur et à mesure des avancées scientifiques. Pour autant, le recours à la classification diagnostique connaît des limites dans la pratique clinique et conduit à un retard diagnostique fréquent. Les mécanismes en jeu dans la relation microbiote-TFI restent également à préciser, y compris les phénomènes neuro-endocriniens impliquant l’axe intestin-cerveau
Section grand public
Retrouvez ici votre espace dédié
en_sources_title
en_sources_text_start en_sources_text_end
Chapitres
A propos de cet article
UNE ÉVOLUTION DE STATUT
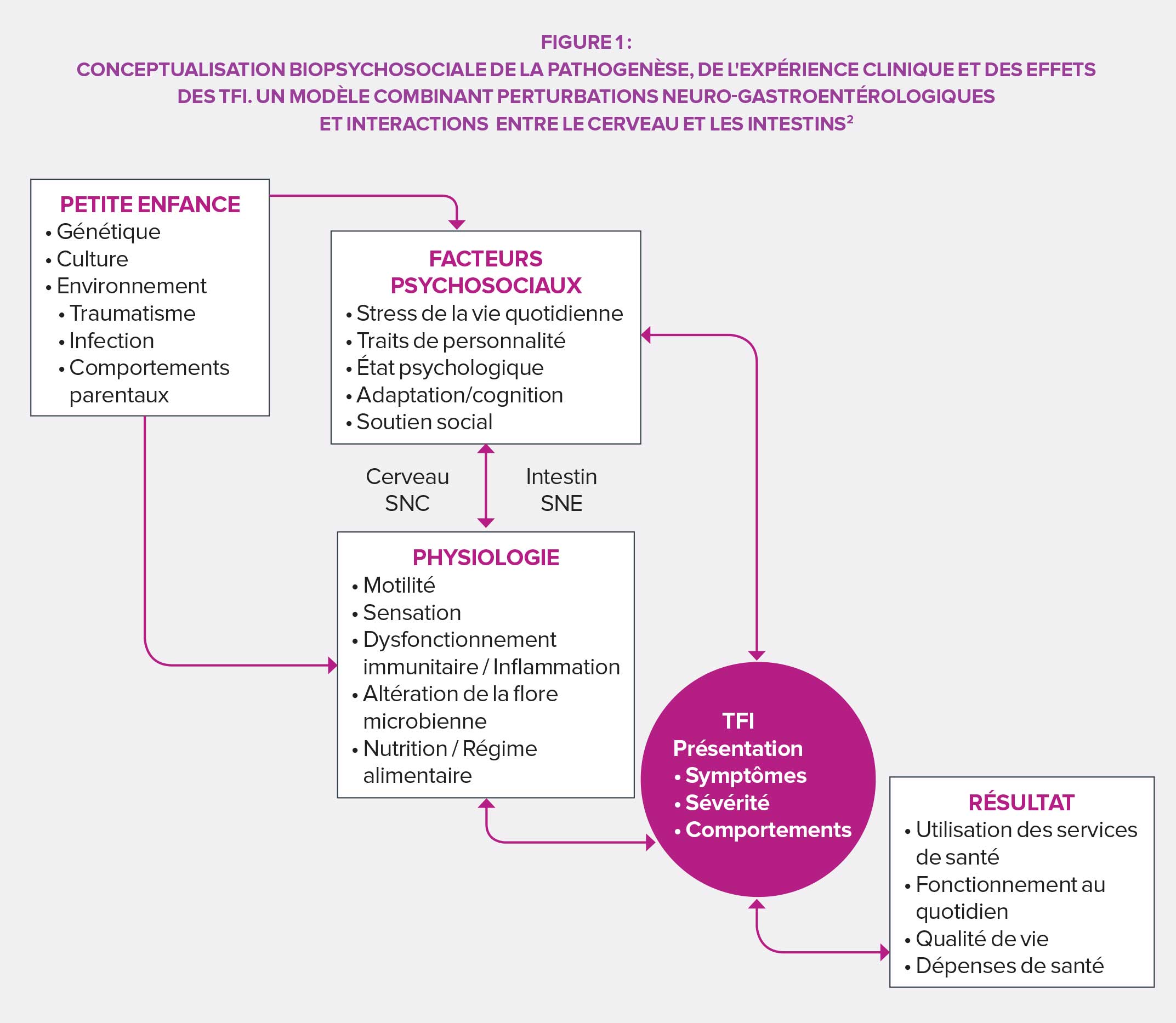
Perçus comme honteux dans un grand nombre de cultures, les troubles fonctionnels intestinaux furent longtemps considérés comme relevant de la vie privée et corrélés au stress et aux émotions davantage qu’à un trouble organique facilement identifiable. Le regard a positivement évolué dans les années 1960 grâce aux progrès techniques et scientifiques : des travaux sur l’étiologie et la physiopathologie ont apporté les fondements d’une compréhension organique des TFI. Les décennies suivantes ont permis pour leur part de se détacher d’une vision « tout physiologique » et d’approfondir les processus psychosociaux connexes avant d’aboutir in fine au modèle biopsychosocial moderne de référence.
ROME, BERCEAU DE LA CLASSIFICATION
Dans la quatrième édition de son ouvrage de référence (Rome IV), la Rome Foundation propose une définition des TFI conçue collaborativement par un collège d’experts : il s’agit de troubles de l’interaction intestin-cerveau, à savoir un « groupe de troubles classés par symptômes gastro-intestinaux, liés à une combinaison de ce qui suit : perturbation de la motilité, hypersensibilité viscérale, altération de la fonction muqueuse et immunitaire, modification du microbiote intestinal et altération des fonctions du système nerveux central (SNC) ». Le fruit de cette réflexion permet non seulement de proposer une catégorisation précise des TFI mais également d’en justifier l’étude et la prise en compte.
53 TFI
Le système de classification Rome IV est fondé sur des critères symptomatiques regroupés par région anatomique (œsophagienne, gastroduodénale, intestinale, biliaire et ano-rectale). Cependant, la localisation symptomatologique à elle seule n’est pas suffisante, particulièrement pour le syndrome de l’intestin irritable (SII en Français, IBS en Anglais pour Irritable Bowel Syndrome), les dyspepsies fonctionnelles ou le syndrome de douleurs abdominales (difficiles à situer et influencées par des effets globaux résultant de la dérégulation des voies de signalisation entre les systèmes nerveux central et entérique) médié par le système nerveux central. Ses 33 entrées pour les adultes et 20 pour les nourrissons, enfants et adolescents assurent un diagnostic précis et facilitent la mise en œuvre d’une prise en charge ciblée. À cet égard, la Rome Foundation insiste sur l’importance de ne pas limiter les approches thérapeutiques à la seule médication et préconise une approche biopsychosociale pour répondre à la variabilité des cas et aux attentes individuelles des patients souffrant de TFI.

LE MICROBIOTE, ACTEUR INTESTINAL MAJEUR3,4
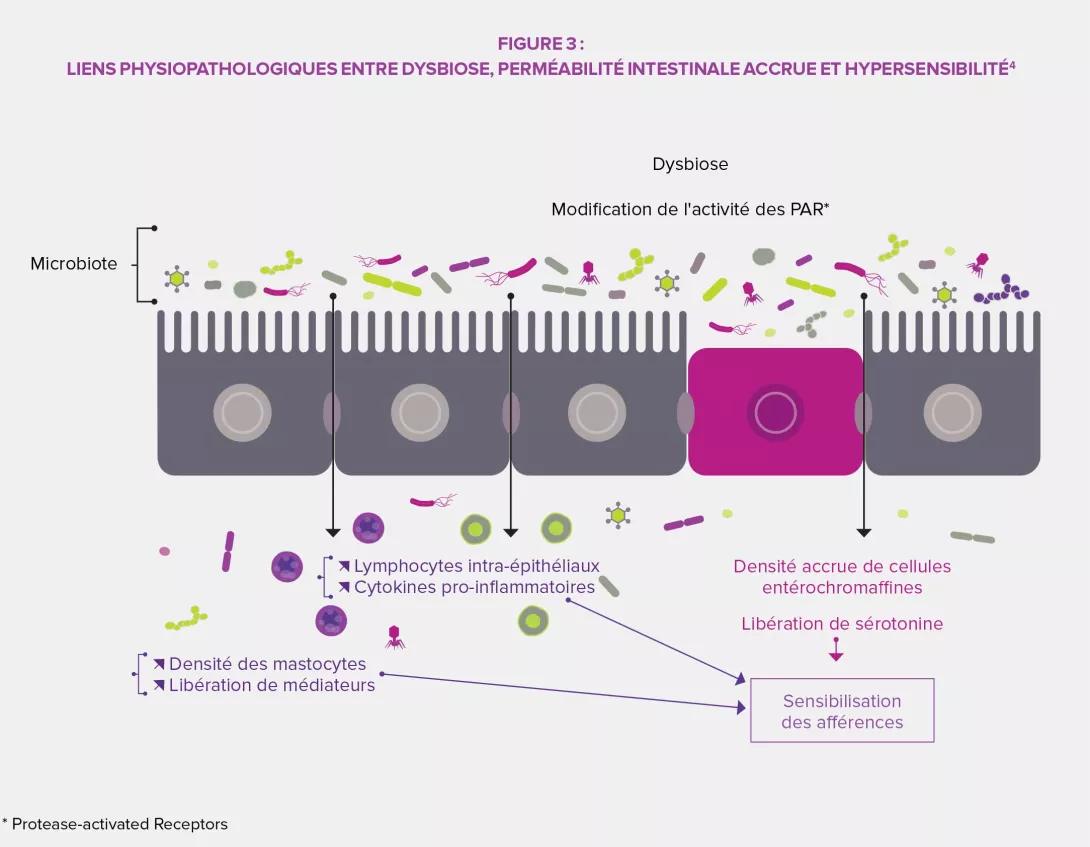
Le microbiote intestinal a une influence complexe sur le métabolisme, la nutrition et les fonctions immunitaires de l’hôte. Son altération joue un rôle central dans les TFI. La dysbiose a particulièrement été étudiée dans le SII et les études chez l’animal ont montré que ce déséquilibre serait impliqué dans l’hypersensibilité viscérale observée (via les acides biliaires endoluminaux), ainsi que dans les troubles moteurs intestinaux par l’expression d’enzymes impliquées dans la synthèse de neuromodulateurs (acide gamma aminobutyrique par exemple) et des produits de fermentation colique (gaz ou acides gras à courte chaîne AGCC). Enfin, la dysbiose favoriserait notamment l’altération de la barrière intestinale : une perméabilité intestinale accrue faciliterait ainsi le passage des antigènes bactériens à l’origine d’une inflammation de bas grade conduisant à une sensibilisation des afférences sensitives du système nerveux entérique.
UNE APPROCHE PROMETTEUSE
L’hétérogénéité des TFI et les résultats contradictoires en termes de composition bactérienne selon les études et les méthodologies employées ne permettent pas encore d’utiliser le microbiote et ses métabolites comme marqueur pertinent pour le diagnostic, le suivi de la progression de la maladie ou la réponse au traitement. La littérature confirme toutefois l’importance de la diversité et de la composition du microbiote intestinal dans la physiopathologie des TFI, et par conséquent l’impact potentiel d’approches liées à des modulations des populations bactériennes intestinales.
4 Marteau P, Doré J. Gut microbiota, a full fledged organ. John Libbey Eurotext. 2017