Focus sur la semaine asie-pacifique des maladies digestives
Retour de congrès
Par le Pr. Uday C Ghoshal
Département de gastro-entérologie, SGPGI, Lucknow, Inde
Section grand public
Retrouvez ici votre espace dédié
en_sources_title
en_sources_text_start en_sources_text_end
Chapitres

A propos de cet article
Auteur
La compréhension du système digestif et des troubles intestinaux s’est récemment améliorée grâce à l’acquisition de connaissances sur le microbiote intestinal (MI) et la dysbiose [1]. Lors de ce congrès, plusieurs aspects du MI ont été présentés et sont évoqués dans cet article.
Description du microbiote intestinal
Considéré comme un véritable organe, le MI comprend 10 fois plus de microorganismes (1014) que de cellules humaines dans notre corps (1013). Il exerce différentes fonctions parmi lesquelles : la digestion des aliments, le métabolisme des médicaments et des toxines, la synthèse de vitamines, un effet de barrière vis-à-vis des bactéries pathogènes, une modulation des fonctions immunitaires, neuro-hormonales et du système nerveux central [2]. Compte tenu de ses nombreuses fonctions, on peut en déduire que son altération est associée à plusieurs maladies et que sa modulation peut être bénéfique.
Rôle du microbiote intestinal dans le cancer colorectal
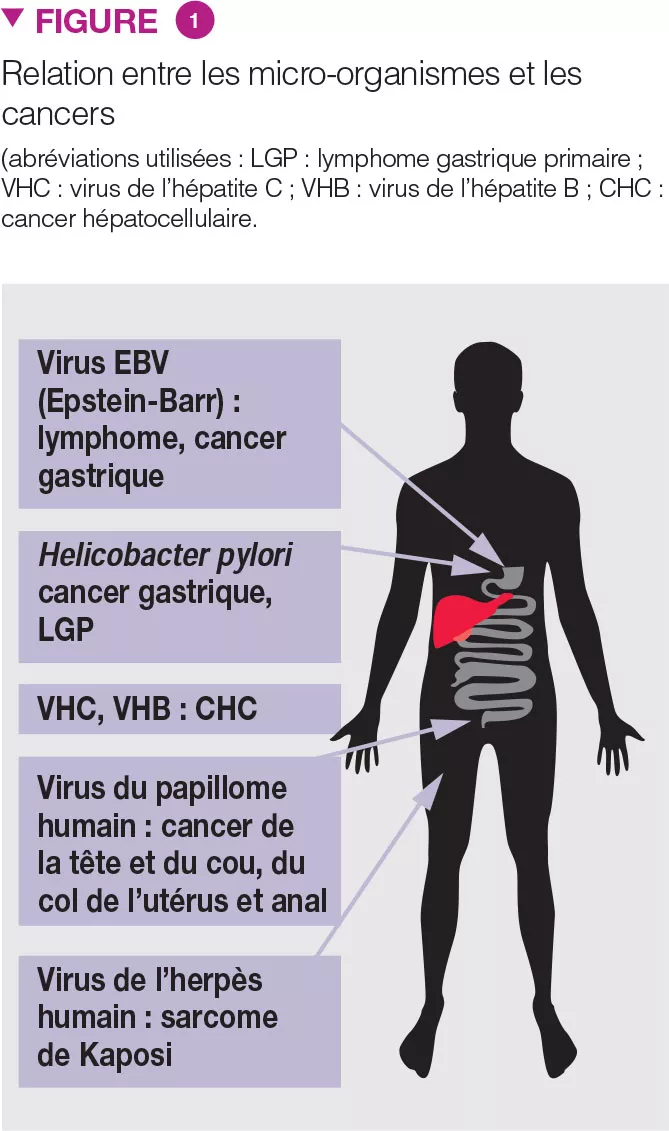
L’association entre microorganismes et cancer est connue (Figure 1) [3]. Des données récentes suggèrent que la dysbiose pourrait jouer un rôle dans le cancer colorectal. Le microbiote fécal des patients présentant une polypose colique ressemble à celui des patients présentant un cancer colorectal. Alors que Clostridium spp., Bacteroides et Bifidobacterium spp. sont associées au cancer colorectal, les bactéries productrices d’acide lactique (par ex. : Lactobacillus spp. ou Eubacterium aerofaciens) sont négativement associées au cancer colorectal. La production de méthane et de H2S (sulfure d’hydrogène) associée au microbiote intestinal, et la présence de Streptococcus bovis pourraient jouer un rôle dans le développement du cancer colorectal. Par ailleurs, il a récemment été suggéré que l’obésité pourrait être liée au MI, et celle-ci constitue un facteur de prédisposition au cancer colorectal.
Microbiote intestinal et obésité
L’extraction des calories des aliments dépend non seulement de la fonction digestive de l’intestin grêle, mais également de l’extraction des calories mal absorbées par le microbiote colique. Alors que la présence de Firmicutes est associée à une extraction plus importante des calories, les Bacteroidetes ont un effet opposé [4]. Il a été démontré que le microbiote fécal des personnes obèses était différent de celui des personnes non obèses. Dans une étude de cohorte rétrospective menée au Royaume-Uni chez 21 714 nourrissons, 1 306 (6 %) sont devenus obèses à l’âge de 4 ans. Selon les analyses de régression logistique tenant compte du contexte familial, l’exposition aux antibiotiques avant l’âge de 2 ans a été associée au développement de l’obésité et le nombre de cycles d’antibiotique était corrélé avec le développement de l’obésité [5].
Autres syndromes métaboliques
La stéatose hépatique non alcoolique (SHNA) et le syndrome métabolique peuvent être associés à une dysbiose, comprenant une augmentation du nombre de bactéries présentes dans la région haute de l’intestin [6]. Une étude non contrôlée et trois études cas-témoins ont montré que la surprolifération bactérienne de l’intestin grêle était associée à une SHNA [6]. Deux études ont montré une plus faible abondance relative de Bacteroidetes, et une plus grande abondance de C. coccoides et de Prevotella chez les patients présentant une SHNA. Une extraction plus importante des calories des glucides complexes non absorbés, une résistance à l’insuline et une production endogène d’alcool peuvent contribuer à la pathogenèse de la SHNA due à la dysbiose. Le MI joue un rôle important dans le métabolisme du glucose, la résistance à l’insuline, le diabète, et a une incidence sur son traitement. Le microbiote fécal des patients atteints de diabète est différent de celui de la population-contrôle [4]. Il a été montré qu’il était un facteur de régulation important de la glycémie après l’ingestion de différents aliments, indépendamment de l’exercice physique, ou du mode de vie [7]. La metformine, un agent hypoglycémique oral, peut en partie agir en altérant le microbiote intestinal. Bien que les études sur le rôle du microbiote dans la coronaropathie soient rares et les résultats mitigés, de nouvelles données suggèrent qu’il pourrait jouer un rôle dans cette maladie.
Usage abusif d’antibiotiques en asie
L’usage d’antibiotiques est important en Asie et la mise en place de politiques encourageant un usage approprié laisse à désirer, avec un risque d’apparition de microorganismes super-résistants aux antibiotiques. Cet usage abusif s’explique par une disponibilité illimitée et des indications non appropriées comme le rhume ou la gastro-entérite aiguë. Les probiotiques, lorsqu’ils sont indiqués, peuvent aider à limiter l’usage abusif d’antibiotiques.
Manipulation du microbiote intestinal par des agents autres que les antibiotiques
Alors que la modulation du microbiote par la rifaximine est bien connue, les probiotiques et la transplantation fécale sont potentiellement intéressants pour prendre en charge les pathologies associées à la dysbiose. Les probiotiques peuvent être prescrits de façon concomitante en cas de traitement d’éradication d’Helicobacter pylori. Des méta-analyses ont montré que l’administration concomitante de probiotiques pouvait restaurer l’eubiose et augmentait [2] les taux d’éradication en raison de la diminution des effets indésirables et d’une meilleure observance [9].
À partir de 23 essais contrôlés randomisés, l’American College of Gastroenterology a recommandé le recours aux probiotiques pour améliorer les ballonnements et flatulences dans le syndrome de l’intestin irritable [8]. Une revue Cochrane a montré l’utilité des probiotiques dans la prévention de la diarrhée associée à Clostridium difficile [9]. Une méta-analyse a montré que les probiotiques à base de plusieurs espèces induisaient et maintenaient une rémission dans la rectocolite hémorragique, alors que les données sur la maladie de Crohn sont limitées [10].
Orientations futures
Dans le but de former un consortium Asie- Pacifique sur le MI, similaire aux groupes européens et nord-américains, et afin d’examiner les données actuelles dans la région Asie-Pacifique, un consensus a été récemment élaboré et publié [9]. Les principales conclusions de ce consensus sont les suivantes : un nombre croissant de données étaye le potentiel thérapeutique des probiotiques dans la modulation des fonctions gastro-intestinales et le soulagement des symptômes de ces troubles, mais d’autres recherches sont nécessaires [9].









